Hôm nay 05/01/2022, Thứ trưởng Nguyễn Trường Sơn đã ký quyết định 29/QĐ-BYT ban hành "Hướng dẫn giám sát phản ứng của thuốc (ADR) tại các cơ sở khám, chữa bệnh". Hướng dẫn này thay thế cho Hướng dẫn ban hành năm 2013 (quyết định 1088) là tài liệu chuyên môn hướng dẫn của Bộ Y tế về triển khai hoạt động Giám sát phản ứng có hại của thuốc, Cảnh giác Dược hướng tới sử dụng thuốc hợp lý, an toàn tại các cơ sở khám chữa bệnh. Hướng dẫn có nhiều điểm cập nhật quan trọng phù hợp với hướng dẫn thực hành Cảnh giác Dược được khuyến cáo bởi Tổ chức Y Tế Thế giới, của các nước có hoạt động Cảnh giác Dược phát triển và phù hợp với các quy định hiện hành theo quy định của Luật Dược và các văn bản dưới luật trong lĩnh vực chuyên ngành. Các phương pháp giám sát ADR tích cực bên cạnh báo cáo ADR tự nguyện kinh điển, các phương pháp đánh giá ADR (khả năng phòng tránh được) và quản lý giảm thiểu nguy cơ liên quan đến thuốc (đặc biệt các thuốc có nguy cơ cao) đã được đề cập trong hướng dẫn hy vọng sẽ giúp định hướng để các bệnh viện từng bước triển khai hoạt động này. Trung tâm DI & ADR Quốc gia, trung tâm DI & ADR khu vực TP Hồ Chí Minh xin chân thành cám ơn sự điều phối, chỉ đạo của lãnh đạo và các anh chị chuyên viên Cục Quản lý Khám, Chữa bệnh, sự đóng góp nhiệt tình các ý kiến chuyên môn của các Thày, Cô, anh chị em đồng nghiệp từ nhiều bệnh viện, các trường Đại học để hướng dẫn được hoàn chỉnh và trình ký ban hành. Link tải hướng dẫn:
ở đây.
BỘ Y TẾ CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập - Tự do - Hạnh phúc
_______________________________________
Số: 29/QĐ-BYT.
Hà Nội, ngày 05 tháng 12 năm 2022. QUYẾT ĐỊNH
Về việc ban hành Hướng dẫn giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Luật Khám bệnh, chữa bệnh năm 2009; Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế; Theo đề nghị của Ban soạn thảo Hướng dẫn giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh được thành lập theo 2987/QĐBYT ngày 18/6/2021 của Bộ trưởng Bộ Y tế tại biên bản họp ngày 02/12/2021; Theo đề nghị của Cục trưởng Cục Quản lý Khám, chữa bệnh.
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này Hướng dẫn giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh.
Điều 2. Hướng dẫn giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh áp dụng tại các cơ sở khám bệnh, chữa bệnh Nhà nước và tư nhân trên cả nước.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký, ban hành. Bãi bỏ Quyết định số 1088/QĐ-BYT/QĐ-BYT ngày 04/4/2013 của Bộ trưởng Bộ Y tế về việc ban hành Hướng dẫn giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh.
Điều 4. Các ông, bà: Cục trưởng Cục Quản lý Khám, chữa bệnh, Chánh Văn phòng Bộ, Chánh Thanh tra Bộ; các Vụ trưởng, Cục trưởng của Bộ Y tế; Giám đốc các cơ sở khám, chữa bệnh trực thuộc Bộ Y tế; Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương; Thủ trưởng y tế các Bộ, ngành; Thủ trưởng các đơn vị có liên quan chịu trách nhiệm thi hành Quyết định này. Nơi nhận: - Như Điều 4; - Bộ trưởng (để báo cáo); - Các Thứ trưởng; - Cổng thông tin điện tử Bộ Y tế, website Cục - QLKCB; - Lưu: VT, KCB.
KT. BỘ TRƯỞNG
THỨ TRƯỞNG.
Nguyễn Trường Sơn.
[caption id="" align="alignnone" widthx="950"]
 HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)
HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)[/caption]
| Chỉ đạo biên soạn |
| PGS.TS. Nguyễn Trường Sơn | Thứ trưởng Bộ Y tế |
| Chủ biên |
| PGS.TS. Lương Ngọc Khuê | Cục trưởng Cục Quản lý Khám, chữa bệnh. |
| Đồng chủ biên |
| TS. Cao Hưng Thái | Phó Cục trưởng Cục Quản lý khám, chữa bệnh. |
| PGS.TS. Nguyễn Hoàng Anh | Giám đốc Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc, Trường Đại học Dược Hà Nội; Phó trưởng khoa Dược, Bệnh viện Bạch Mai. |
| Tham gia biên soạn và thẩm định |
| PGS.TS. Nguyễn Văn Đoàn | Nguyên Giám đốc Trung tâm Dị ứng-Miễn dịch lâm sàng, Bệnh viện Bạch Mai. |
| TS. Nguyễn Quốc Bình | Giám đốc Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc khu vực Thành phố Hồ Chí Minh, Trưởng khoa Dược Bệnh viện Chợ Rẫy |
| TS. Nguyễn Hữu Chiến | Trưởng phòng Kế hoạch Tổng hợp, Viện Huyết học và truyền máu Trung ương |
| DSCKII. Trần Thị Đảm | Trưởng Khoa Dược, Bệnh viện Đà Nẵng |
| ThS. Nguyễn Thị Phương Lan | Phó trưởng Phòng Quản lý Dược cổ truyền, Cục Quản lý Y, Dược cổ truyền |
| TS. Vũ Đình Hòa | Phó Giám đốc Trung Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc, Trường Đại học Dược Hà Nội |
| ThS. Châu Thị Ánh Minh | Phó giám đốc Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc khu vực Thành phố Hồ Chí Minh, Bệnh viện Chợ Rẫy |
| ThS. Nguyễn Thu Minh | Phó trưởng Khoa Dược, Bệnh viện Bạch Mai |
| ThS. Phạm Thu Hà | Phó trưởng khoa Dược, Bệnh viện Nhi Trung ương |
| ThS. Đinh Thu Hương | Phó Trưởng Khoa Dược, Bệnh viện Phổi Trung ương |
| ThS. Phạm Hồng Thắm | Phó trưởng Khoa Dược, Bệnh viện Nhân dân Gia Định |
| CNĐD. Lê Thị Thái Vân | Phó trưởng Phòng Điều dưỡng, Bệnh viện Phụ sản Trung ương |
| ThS. Lê Kim Dung | Chuyên viên chính Phòng Nghiệp vụ - Thanh tra - Bảo vệ sức khỏe cán bộ, Cục Quản lý khám, chữa bệnh |
| ThS. Dương Thị Hải Ngọc | Chuyên viên chính, Vụ Sức khoẻ Bà mẹ và Trẻ em |
| ThS. Nguyễn Thanh Hường | Chuyên viên Phòng Đăng ký thuốc, Cục Quản lý Dược |
| TS. Nguyễn Như Hồ | Giảng viên chính Bộ môn Dược lâm sàng, Khoa Dược Đại học Y Dược Thành phồ Hồ Chí Minh |
| ThS. Nguyễn Duy Tám | Khoa Dược, Bệnh viện Trung ương Quân đội 108 |
| ThS. Dương Thanh Hải | Khoa Dược, Bệnh viện Đa khoa Quốc tế Vinmec Times City |
| ThS. Nguyễn Hoàng Linh Đan | Khoa Dược, Bệnh viện Từ Du |
| DS. Nguyễn Thị Trang | Khoa Dược, Bệnh viện Đại học Y Dược Thành phố Hồ Chí Minh |
| Tổ thư ký và biên tập |
| ThS. Lê Kim Dung | Chuyên viên chính Cục Quản lý khám, chữa bệnh |
| ThS. Trần Ngân Hà | Chuyên viên Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc, Trường Đại học Dược Hà Nội |
| DS. Đỗ Thị Ngát | Chuyên viên Phòng Nghiệp vụ - Thanh tra - Bảo vệ sức khỏe cán bộ, Cục Quản lý khám, chữa bệnh |
| Trung tâm DI & ADR Quốc gia, Trường Đại học Dược Hà Nội |
Mục lục
DANH SÁCH BAN BIÊN SOẠN ........................................................................3 MỤC LỤC .............................................................................................................5 DANH MỤC KÝ HIỆU VÀ CHỮ VIẾT TẮT ....................................................6 1. GIẢI THÍCH TỪ NGỮ .....................................................................................7 2. MỤC ĐÍCH CỦA HOẠT ĐỘNG GIÁM SÁT ADR ......................................8 3 .NỘI DUNG THỰC HIỆN ..............................................................................8
- 3.1. Phân công bộ phận/người phụ trách giám sát ADR ................................... 8
- 3.2. Xây dựng và triển khai quy trình giám sát ADR ........................................ 9
- 3.2 Phát hiện ADR .......................................................................................... 10
- 3.3 Báo cáo ADR ............................................................................................ 13
- 3.4 Đánh giá ADR .......................................................................................... 19
- 3.5 Dự phòng ADR ......................................................................................... 23
-
4. TỔ CHỨC THỰC HIỆN ............................................................................. 30
- 4.1 Người đứng đầu cơ sở khám bệnh, chữa bệnh ......................................... 30
- 4.2. Tiểu ban giám sát ADR - Hội đồng Thuốc và điều trị/Bộ phận Dược lâm sàng tại cơ sở khám bệnh, chữa bệnh không tổ chức khoa Dược ................... 30
- 4.3 Khoa Dược ................................................................................................ 31
- 4.4 Phòng Quản lý chất lượng ........................................................................ 32 5.
- 4.5 Phòng Kế hoạch tổng hợp ......................................................................... 32
- 4.6 Khoa lâm sàng, khoa, phòng khám bệnh và khoa cận lâm sàng .............. 32
- 4.7 Nhân viên y tế ........................................................................................... 33
CÁC PHỤ LỤC .................................................................................................. 34 PHỤ LỤC 1. Phân loại khuyến cáo thực hiện hoạt động giám sát ADR ................................................................................................................... 34 PHỤ LỤC 2. Một số biểu hiện lâm sàng và cận lâm sàng bất thường có thể liên quan đến phản ứng có hại của thuốc .................................................................. 35 PHỤ LỤC 3. Mẫu báo cáo phản ứng có hại của thuốc................................................ 37 PHỤ LỤC 4. Ví dụ mẫu báo cáo ADR có chủ đích........................................... 39 PHỤ LỤC 5. Danh sách một số thuốc, xét nghiệm và biểu hiện lâm sàng là dấu hiệu phát hiện ADR ............................................................................................ 39 PHỤ LỤC 6. Sơ đồ phân loại sai sót liên quan đến thuốc ............................................. 41 PHỤ LỤC 7. Thang đánh giá mối liên quan giữa thuốc và ADR ..................... 42 PHỤ LỤC 8. Thang đánh giá khả năng phòng tránh được của ADR ............... 45 PHỤ LỤC 9. Thang đánh giá chất lượng của báo cáo ADR ....................................... 49 PHỤ LỤC 10. Những điểm cần lưu ý trong quá trình sử dụng thuốc để giảm thiểu khả năng xuất hiện ADR .................................................................................... 51 PHỤ LỤC 11. Danh sách một số đối tượng người bệnh và thuốc có nguy cơ cao xuất hiện ADR .................................................................................................................... 53 PHỤ LỤC 12. Hướng dẫn quản lý thuốc có nguy cơ cao ............................................. 55 PHỤ LỤC 13. Đánh giá hiệu quả hoạt động giám sát ADR trong cơ sở khám bệnh, chữa bệnh ........................................................................................................... 66
DANH MỤC KÝ HIỆU VÀ CHỮ VIẾT TẮT
| ADR | Adverse Drug Reaction | Phản ứng có hại của thuốc |
| AE | Adverse Event | Biến cố bất lợi |
| aPTT | Activated Partial Thromboplastin Time | Thời gian hoạt hoá bán phần thromboplastin |
| AST | Aspartate transaminase | |
| ALT | Alanine transaminase | |
| ALP | Alkaline phosphatase | |
| CTCAE | Common Terminology Criteria for Adverse Events | Hệ thống thuật ngữ biến cố bất lợi chuẩn hoá thông dụng |
| INR | International normalized ratio | Chỉ số chuẩn hóa quốc tế |
| ME | Medication error | Sai sót liên quan đến thuốc |
| NCC MERP | National Coordinating Council for Medication Error Reporting and Prevention | Hội đồng điều phối Quốc gia Hoa Kỳ về báo cáo và phòng tránh sai sót liên quan đến thuốc |
| pADR | Preventable Adverse Drug Reaction | Phản ứng có hại của thuốc có thể phòng tránh được |
| SAE | Serious Adverse Event | Biến cố bất lợi nghiêm trọng |
| Trung tâm DI&ADR Quốc gia | | Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc |
| UMC | Uppsala Monitoring Centre | Trung tâm giám sát thuốc toàn cầu Uppsala của Tổ chức Y tế Thế giới |
| WHO | World Health Organization | Tổ chức Y tế thế giới |
HƯỚNG DẪN Hoạt động giám sát phản ứng có hại của thuốc (ADR) tại các cơ sở khám bệnh, chữa bệnh
(Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022 của Bộ trưởng Bộ Y tế). Phản ứng có hại của thuốc là một trong những nguyên nhân làm tăng tỷ lệ mắc bệnh, tỷ lệ tử vong, kéo dài thời gian nằm viện, giảm tuân thủ điều trị và tăng chi phí điều trị cho người bệnh. Vì vậy, việc giám sát phản ứng có hại của thuốc đóng vai trò quan trọng nhằm giảm thiểu những nguy cơ liên quan đến thuốc, đảm bảo an toàn trong quá trình sử dụng thuốc của người bệnh. Việc giám sát phản ứng có hại của thuốc bao gồm: phát hiện, xử trí, báo cáo, đánh giá và dự phòng các biến cố bất lợi liên quan đến thuốc. Bộ Y tế ban hành hướng dẫn này với mục tiêu:
- Nâng cao nhận thức về vấn đề an toàn trong sử dụng thuốc và khuyến khích các cơ sở khám bệnh, chữa bệnh, nhân viên y tế báo cáo phản ứng có hại của thuốc như là nhiệm vụ chuyên môn trong thực hành lâm sàng và là một phần trách nhiệm, đạo đức nghề nghiệp.
- Phát hiện sớm các vấn đề an toàn thuốc, kịp thời xử trí và chủ động thực hiện các biện pháp dự phòng các biến cố bất lợi xảy ra trong quá trình sử dụng thuốc trên người bệnh, tăng cường việc sử dụng thuốc hợp lý, giảm tỷ lệ mắc bệnh và tỷ lệ tử vong liên quan đến thuốc trong thực hành lâm sàng.
I. GIẢI THÍCH TỪ NGỮ
- Phản ứng có hại của thuốc (ADR):
- Theo Luật Dược năm 2016, phản ứng có hại của thuốc (Adverse Drug Reactions - ADR) là phản ứng không mong muốn, có hại đến sức khỏe, có thể xảy ra ở liều dùng bình thường.
- Theo định nghĩa của Tổ chức Y tế thế giới, phản ứng có hại của thuốc là phản ứng độc hại, không định trước và xuất hiện ở liều thường dùng cho người với mục đích phòng bệnh, chẩn đoán, điều trị bệnh hoặc làm thay đổi chức năng sinh lý của cơ thể.
- Biến cố bất lợi (AE) là bất kỳ tổn hại nào xảy ra trong quá trình sử dụng thuốc, vắc xin và sinh phẩm khi điều trị nhưng không nhất thiết là do phác đồ điều trị gây ra. - Phản ứng có hại của thuốc phòng tránh được (pADR) là tổn thương gây ra bởi một sai sót ở bất kỳ giai đoạn nào trong quá trình sử dụng thuốc. - Sai sót liên quan đến thuốc (ME) là bất kỳ biến cố có thể phòng tránh nào có khả năng gây ra hoặc dẫn đến việc sử dụng thuốc không hợp lý, hoặc gây hại cho người bệnh trong khi thuốc được kiểm soát bởi nhân viên y tế, người bệnh, hoặc người sử dụng. - Thuốc có nguy cơ cao là thuốc có khả năng cao gây hại cho người bệnh khi có sai sót trong quá trình sử dụng thuốc. Các thuốc có nguy cơ cao bao gồm thuốc có khoảng điều trị hẹp và thuốc có nguy cơ cao gây hại cho người bệnh khi sử dụng sai đường dùng hoặc có sai sót trong chu trình quản lý và sử dụng thuốc.
II. MỤC ĐÍCH CỦA HOẠT ĐỘNG GIÁM SÁT ADR
- Cải thiện chất lượng chăm sóc và điều trị người bệnh và giảm thời gian nằm viện thông qua đảm bảo sử dụng thuốc an toàn và hợp lý. - Truyền thông và giáo dục cho nhân viên y tế và người bệnh về tác dụng của thuốc và nâng cao nhận thức về ADR. - Cung cấp thang đánh giá gián tiếp về chất lượng điều trị bằng thuốc thông qua việc xác định các ADR tiềm tàng và giám sát thuốc có nguy cơ cao hoặc người bệnh có nguy cơ cao. - Bổ sung các hoạt động quản lý nguy cơ và giảm thiểu nguy cơ liên quan đến thuốc tại đơn vị. - Đánh giá tính an toàn của các phương pháp điều trị bằng thuốc. - Cung cấp dữ liệu điều tra, nghiên cứu đảm bảo chất lượng để xác định triển khai đánh giá sử dụng thuốc hoặc các can thiệp cải thiện hiệu quả sử dụng thuốc hợp lý, an toàn khác. - Xác định tỷ lệ gặp ADR và các đặc điểm liên quan.
III. NỘI DUNG THỰC HIỆN
Chương trình giám sát ADR là một trong các nội dung quan trọng trong chu trình sử dụng thuốc của cơ sở khám bệnh, chữa bệnh. Có 06 nhiệm vụ chính trong hoạt động giám sát ADR tại cơ sở khám bệnh, chữa bệnh bao gồm:
- Phân công bộ phận/người phụ trách giám sát ADR.
- Xây dựng và triển khai quy trình giám sát ADR.
- Phát hiện ADR.
- Báo cáo ADR.
- Đánh giá ADR.
- Dự phòng ADR.
Tùy vào điều kiện các cơ sở khám bệnh, chữa bệnh có thể triển khai các hoạt động giám sát ADR như khuyến cáo tại Phụ lục 1.
3.1. Phân công bộ phận/người phụ trách giám sát ADR
- Đối với các bệnh viện, Tiểu ban giám sát ADR theo quy định tại Điều 12 Thông tư số 21/2013/TT-BYT ngày 08 tháng 8 năm 2013 của Bộ Y tế Quy định về tổ chức và hoạt động của Hội đồng Thuốc và điều trị trong bệnh viện có trách nhiệm triển khai giám sát ADR tại bệnh viện. Thành phần trong Tiểu ban giám sát ADR có thể bao gồm: lãnh đạo bệnh viện (Trưởng Tiểu ban), đại diện khoa Dược (ưu tiên dược sĩ làm công tác dược lâm sàng), đại diện phòng Điều dưỡng, đại diện phòng Kế hoạch tổng hợp, đại diện phòng Quản lý chất lượng, đại diện các Khoa lâm sàng và thành viên khác (nếu có, ví dụ: công nghệ thông tin). - Đối với các cơ sở khám bệnh, chữa bệnh khác, người chịu trách nhiệm chuyên môn của cơ sở khám bệnh, chữa bệnh thực hiện hoặc phân công nhiệm vụ cụ thể cho nhân viên y tế (bộ phận Dược lâm sàng) phụ trách hoạt động giám sát ADR tại đơn vị.
3.2. Xây dựng và triển khai quy trình giám sát ADR
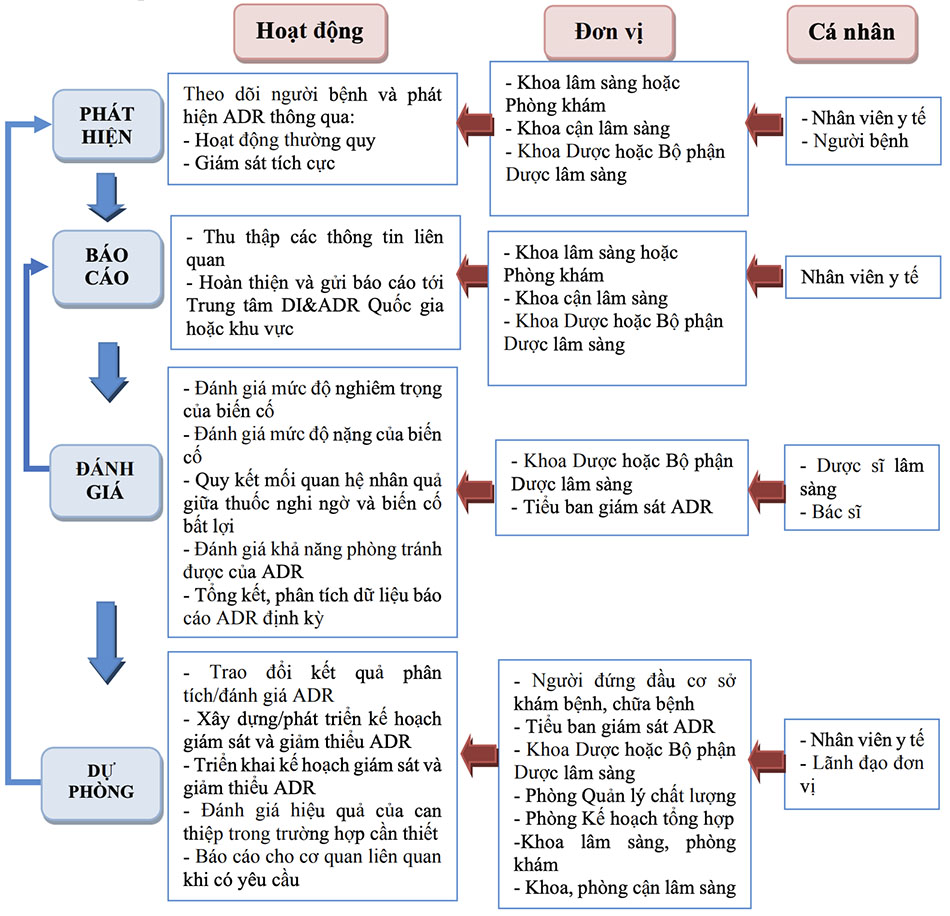
- Việc xây dựng và triển khai quy trình giám sát ADR có vai trò quan trọng trong việc tăng cường hoạt động báo cáo ADR trong cơ sở khám bệnh, chữa bệnh. Trong đó, dược sĩ lâm sàng (hoặc nhân viên y tế khác được người đứng đầu cơ sở khám bệnh, chữa bệnh phân công) là đầu mối xây dựng và triển khai quy trình này. Quy trình giám sát ADR cần được xây dựng phù hợp với điều kiện của từng cơ sở điều trị với các nội dung chính bao gồm: phát hiện, báo cáo, đánh giá và dự phòng ADR (xem Hình 1). - Để triển khai hiệu quả quy trình giám sát ADR trong cơ sở khám bệnh, chữa bệnh cần đảm bảo sự cam kết của người đứng đầu cơ sở khám bệnh, chữa bệnh, các phòng chức năng và các khoa lâm sàng, đảm bảo sự phối hợp đa ngành, phối hợp hoạt động báo cáo - phản hồi cho người báo cáo và ra quyết định phù hợp (xem Phần IV). Ngoài ra, khuyến khích các đơn vị đa dạng hóa các cách tiếp cận, áp dụng công nghệ thông tin để hoạt động giám sát ADR được triển khai kịp thời, hiệu quả.
3.3. Phát hiện ADR
Việc phát hiện các biến cố bất lợi liên quan đến thuốc và nguyên nhân gây ra biến cố bất lợi là bước đầu tiên trong hoạt động giám sát ADR nhằm cải thiện an toàn người bệnh thông qua xây dựng các chiến lược dự phòng và tối ưu hóa việc sử dụng thuốc trong mỗi giai đoạn của quy trình khám bệnh, chữa bệnh.
3.3.1. Phát hiện ADR thông qua hoạt động thường quy
- Theo dõi và ghi nhận lại những biểu hiện lâm sàng và cận lâm sàng bất thường xảy ra trên người bệnh dựa trên các thông tin do người bệnh cung cấp và các triệu chứng ghi nhận được trong quá trình chăm sóc, điều trị và theo dõi người bệnh (xem Phụ lục 2). - Kiểm tra lại tất cả các thuốc thực tế người bệnh đã dùng. - Kiểm tra chất lượng cảm quan mẫu thuốc được lưu lại xem có biểu hiện gì về chất lượng thuốc. - Kiểm tra lại một số thông tin sau:
- + Người bệnh có tiền sử dị ứng, đặc biệt là dị ứng thuốc không?
- + Việc sử dụng thuốc có phù hợp tình trạng bệnh lý, có cân nhắc đến các bệnh mắc kèm và chống chỉ định trên người bệnh hay không?
- + Liều dùng thuốc đã theo như khuyến cáo chưa?
- Xem xét sự phù hợp về thời điểm dùng thuốc nghi ngờ và thời điểm xuất hiện ADR. - Xác định diễn biến phản ứng có hại sau khi ngừng sử dụng và tái sử dụng thuốc nghi ngờ (nếu có):
- + Nếu ngừng sử dụng thuốc nghi ngờ, phản ứng được cải thiện thì đây là một tín hiệu mạnh cho thấy có thể có mối liên quan giữa thuốc nghi ngờ và phản ứng có hại.
- + Nếu tái sử dụng thuốc nghi ngờ (sau khi đã ngừng sử dụng và phản ứng cải thiện), phản ứng có hại xuất hiện lại cũng là một tín hiệu mạnh cho thấy có mối liên quan giữa thuốc nghi ngờ và phản ứng có hại. Tuy nhiên, việc tái sử dụng thuốc nghi ngờ cần được cân nhắc rất cẩn thận để đảm bảo lợi ích của việc dùng lại thuốc vượt trội hơn so với nguy cơ xuất hiện lại phản ứng có hại trên người bệnh và trong điều kiện sẵn sàng phát hiện, xử trí kịp thời tai biến liên quan đến thuốc có thể xảy ra.
- Kiểm tra lại xem phản ứng có hại được ghi nhận đã từng xảy ra với thuốc nghi ngờ hay chưa? có liên quan đến tác dụng dược lý đã biết của thuốc không?
3.3.2. Phát hiện ADR thông qua giám sát tích cực
Có nhiều cách tiếp cận khác nhau để khuyến khích nhân viên y tế phát hiện và báo cáo một cách tự nguyện các vấn đề liên quan đến thuốc (báo cáo ADR), tuy nhiên tình trạng “báo cáo thiếu” vẫn rất phổ biến nên cần có các phương pháp bổ sung phát hiện các biến cố liên quan đến thuốc trong toàn bộ chu trình sử dụng thuốc, kể cả khi biến cố liên quan đến thuốc chưa tác động tới người bệnh (biến cố bất lợi tiềm tàng của thuốc). Khảo sát các biến cố bất lợi tiềm tàng của thuốc giúp xác định biến cố xảy ra ở khâu nào trong hệ thống và xác định khâu nào trong hệ thống kiểm soát đã hoạt động hiệu quả hoặc chưa hiệu quả. Bên cạnh phát hiện và báo cáo ADR tự nguyện, các phương pháp giám sát tích cực thường được sử dụng trong cơ sở khám bệnh, chữa bệnh bao gồm giám sát có chủ đích, giám sát thông qua bộ công cụ tín hiệu phát hiện ADR, rà soát toàn bộ bệnh án, quan sát trực tiếp và hoạt động của dược sĩ tại khoa lâm sàng. Tuy nhiên, không có phương pháp nào có thể phát hiện tất cả các biến cố liên quan đến thuốc mà thường có giá trị bổ sung cho nhau. Do đó, cơ sở khám bệnh, chữa bệnh có thể cân nhắc triển khai một hoặc một số phương pháp phát hiện biến cố bất lợi liên quan đến thuốc phù hợp với điều kiện thực tế của đơn vị mình.
a) Giám sát có chủ đích - Giám sát có chủ đích được thực hiện dựa trên nguyên tắc của báo cáo tự nguyện. Khác với báo cáo tự nguyện, thay vì yêu cầu nhân viên y tế ghi nhận về tất cả các phản ứng có hại xảy ra với tất cả các thuốc và mọi đối tượng người bệnh, giám sát có chủ đích chỉ tập trung theo dõi và báo cáo theo một số tiêu chí nhất định như theo dõi trên một nhóm người bệnh cụ thể, một số phản ứng có hại cụ thể của một số thuốc hay phác đồ điều trị. Giám sát có chủ đích giữ được các ưu điểm của phương pháp báo cáo tự nguyện (chi phí thấp, dễ áp dụng), đồng thời giúp tập trung vào đối tượng cần theo dõi, nâng cao chất lượng báo cáo và giảm bớt khối lượng công việc cho nhân viên y tế so với báo cáo tự nguyện. - Các bước triển khai giám sát ADR có chủ đích như sau:
- + Xác định đối tượng cần giám sát (ví dụ: người bệnh nhiễm HIV/AIDS, người bệnh mắc bệnh lao, bệnh nhi, phụ nữ mang thai…), ADR cần giám sát (ví dụ: phản ứng trên da, phản ứng trên thần kinh trung ương và tâm thần, độc tính trên gan, độc tính trên thận…) hoặc thuốc/nhóm thuốc cần giám sát.
- + Xây dựng biểu mẫu báo cáo ADR có chủ đích (xem Phụ lục 4).
- + Xây dựng quy trình giám sát ADR có chủ đích. + Xác định cỡ mẫu và thời gian giám sát.
- + Tập huấn cho nhân viên y tế tham gia hoạt động giám sát có chủ đích.
- + Triển khai giám sát có chủ đích, lồng ghép vào hoạt động thường quy (nếu có thể).
- + Tổng kết, đánh giá và triển khai các hoạt động chuyên môn để giảm thiểu ADR.
b) Giám sát thông qua bộ công cụ tín hiệu phát hiện ADR Phương pháp rà soát bệnh án thông qua bộ công cụ phát hiện tín hiệu biến cố bất lợi của thuốc (trigger tool) sử dụng kỹ thuật lấy mẫu đủ hiệu lực để xác định các biến cố bất lợi tiềm tàng. Mỗi công cụ là tập hợp một số lượng hữu hạn các tín hiệu phát hiện các loại biến cố bất lợi thường gặp nhất hoặc những biến cố thường gây ra các tổn thương nghiêm trọng. Các tín hiệu được lựa chọn dựa trên tổng quan y văn, ý kiến chuyên gia và kiểm định độ tin cậy. Với mỗi chuyên khoa khác nhau có thể sử dụng các tín hiệu khác nhau. Khi phát hiện được một tín hiệu, các thông tin liên quan sẽ được xem xét để xác định liệu có một biến cố bất lợi đã xảy ra hay không. Có 3 loại tín hiệu:
- Sử dụng một thuốc giải độc (antidote) đặc hiệu để xử trí biến cố bất lợi của thuốc (ví dụ: sử dụng vitamin K để điều trị quá liều chống đông kháng vitamin K; kê đơn flumazenil trong trường hợp an thần quá mức khi dùng thuốc an thần, gây ngủ nhóm benzodiazepin; kê đơn naloxon trong trường hợp quá liều thuốc giảm đau opioid; kê đơn natri polystyrene trong trường hợp tăng kali máu liên quan đến suy thận hoặc do thuốc; sử dụng các thuốc kháng histamin, adrenalin, corticosteroid để xử trí phản vệ do thuốc).
- Kết quả từ các xét nghiệm có thể chỉ ra một biến cố bất lợi do thuốc (ví dụ: xét nghiệm tìm kháng nguyên Clostridium difficile trong phân, xét nghiệm đánh giá chức năng gan (AST, ALT, ALP, bilirubin), xét nghiệm Guaiac tìm kiếm máu ẩn trong phân, thời gian prothrombin (PT), thời gian hoạt hóa bán phần thromboplastin (aPTT), chỉ số INR, số lượng tiểu cầu, nồng độ creatinin huyết thanh, nồng độ thuốc trong huyết thanh, protein niệu…).
- Các biểu hiện lâm sàng gợi ý có thể liên quan đến biến cố bất lợi do thuốc. Tham khảo “Danh sách một số thuốc, xét nghiệm và biểu hiện là dấu hiệu phát hiện ADR” (xem Phụ lục 5).
c) Rà soát toàn bộ bệnh án - Rà soát toàn bộ bệnh án bao gồm xem xét toàn bộ hồ sơ bệnh án tại thời điểm phân tích hoặc hồi cứu lại thông tin. Hoạt động này không chỉ giới hạn trên hồ sơ bệnh án mà còn bao gồm phiếu tổng kết ra viện, cơ sở dữ liệu của khoa Dược và các thông tin về xét nghiệm cận lâm sàng lưu trữ tại các khoa xét nghiệm. Việc rà soát được thực hiện bởi nhân viên y tế đã qua đào tạo. - Phương pháp này có thể áp dụng để phát hiện mọi loại sự cố, mặc dù thường được sử dụng trong phát hiện các biến cố bất lợi và các biến cố bất lợi tiềm tàng do thuốc xảy ra trong quy trình kê đơn và giám sát điều trị. - Phương pháp này ít có hiệu quả trong phát hiện các sai sót của quy trình cấp phát và sử dụng thuốc, trừ khi các sai sót này đã gây tổn hại trên người bệnh.
d) Quan sát trực tiếp Phương pháp này bao gồm quan sát về sử dụng thuốc ngay tại giường bệnh nhằm phát hiện bất cứ khác biệt nào giữa việc sử dụng thuốc cho người bệnh và y lệnh. Đây là phương pháp tin cậy và hiệu quả nhất nhằm phát hiện và thống kê các vấn đề liên quan đến thuốc bao gồm cả các vấn đề khi cấp phát thuốc. Tuy nhiên, phương pháp này yêu cầu nhiều nguồn lực, cần người quan sát được đào tạo kỹ lưỡng và thường không hiệu quả để phát hiện các sai sót trong quá trình kê đơn và giám sát điều trị.
đ) Hoạt động của dược sĩ lâm sàng tại khoa lâm sàng, khoa, phòng khám bệnh - Dược sĩ lâm sàng cần phát huy vai trò trong giám sát và thúc đẩy việc sử dụng thuốc hợp lý, phối hợp cùng các đồng nghiệp lâm sàng để phát hiện các vấn đề về thuốc, đề xuất các tiêu chuẩn và giám sát thực hành sử dụng thuốc. - Báo cáo về các can thiệp của dược sĩ có thể giúp phát hiện và lượng giá các nguy cơ liên quan đến thuốc và thông qua theo dõi các thay đổi bất thường trong thời gian điều trị. Phương pháp này hiệu quả trong phát hiện các sai sót liên quan đến thuốc trong quy trình kê đơn, cả các sai sót tiềm tàng trước khi tác động trên người bệnh, có thể được sử dụng trong phát hiện các sai sót liên quan đến thuốc và các biến cố bất lợi tiềm tàng của thuốc. - Báo cáo can thiệp cũng được sử dụng trong đánh giá hiệu quả của các hệ thống kê đơn điện tử, thông qua đo lường tần suất và loại can thiệp của dược sĩ. - Phương pháp này dễ dàng áp dụng, nhưng có thể gặp khó khăn trong việc quản lý quỹ thời gian của các dược sĩ. Nếu phải thực hiện quá nhiều can thiệp, dược sĩ sẽ không có đủ thời gian để ghi lại tất cả các can thiệp đó.
3.4. Báo cáo ADR
3.4.1. Đối tượng viết báo cáo
a) Người trực tiếp viết báo cáo ADR là bác sĩ, dược sĩ, điều dưỡng viên, hộ sinh viên, kỹ thuật viên và các nhân viên y tế khác. Khuyến khích sự phối hợp của các nhân viên y tế trong việc hoàn thiện báo cáo. b) Thông tin về người báo cáo, bệnh nhân và đơn vị báo cáo ghi trong phiếu báo cáo phản ứng có hại của thuốc được các Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc bảo mật theo quy định hiện hành.
3.4.2. Các trường hợp cần báo cáo
a) Báo cáo tất cả các biến cố bất lợi xảy ra trong quá trình điều trị nghi ngờ là phản ứng có hại gây ra bởi: - Thuốc hóa dược, thuốc dược liệu, thuốc cổ truyền, vắc xin và sinh phẩm.
- Dược liệu, vị thuốc cổ truyền.
b) Ưu tiên báo cáo: - Các phản ứng có hại nghiêm trọng (các phản ứng có hại dẫn đến một trong những hậu quả sau: tử vong; đe dọa tính mạng; buộc người bệnh phải nhập viện để điều trị hoặc kéo dài thời gian nằm viện của người bệnh; để lại di chứng nặng nề hoặc vĩnh viễn cho người bệnh; gây dị tật bẩm sinh ở thai nhi; hoặc bất kỳ phản ứng có hại được nhân viên y tế nhận định là gây ra hậu quả nghiêm trọng về mặt lâm sàng). Trong đó, bao gồm cả các trường hợp ghi nhận tai biến nặng sau tiêm chủng vắc xin. Lưu ý, tất cả các trường hợp phản vệ xảy ra sau khi dùng thuốc cần được báo cáo theo quy định của Thông tư số 51/2017/TT-BYT về việc “Hướng dẫn phòng, chẩn đoán và xử trí phản vệ”. - Phản ứng có hại của thuốc xảy ra trên bệnh nhân nhi, người bệnh cao tuổi, phụ nữ có thai và phụ nữ cho con bú. - Phản ứng có hại của các hoạt chất hoặc thuốc mới được sử dụng tại cơ sở khám bệnh, chữa bệnh. - Phản ứng có hại mới, chưa được biết đến với thuốc (chưa được mô tả trong tờ hướng dẫn sử dụng thuốc, Dược thư Quốc gia Việt Nam, MIMS, Vidal hay các tài liệu tham khảo thông tin thuốc khác). - Phản ứng có hại xảy ra liên tục với một thuốc hoặc một lô thuốc trong thời gian ngắn tại cơ sở khám bệnh, chữa bệnh. - Phản ứng có hại xảy ra liên quan thất bại điều trị, sử dụng thuốc không đạt hiệu lực mong muốn. - Phản ứng có hại xảy ra liên quan đến tương tác thuốc hay quá liều thuốc.
c) Khuyến khích nhân viên y tế báo cáo các vấn đề về chất lượng thuốc và sai sót trong sử dụng thuốc. 3.4.3. Thời gian gửi báo cáo
a) Báo cáo cần được gửi trong thời gian sớm nhất có thể sau khi phát hiện ra phản ứng, ngay cả khi thông tin thu được chưa đầy đủ (báo cáo ban đầu). Trong trường hợp này, có thể bổ sung báo cáo nếu thu thập được thêm thông tin (báo cáo bổ sung). b) Báo cáo trong khi người bệnh chưa xuất viện giúp khai thác đủ thông tin, thực hiện các xét nghiệm cần thiết để xác định nguyên nhân gây ADR. c) Bảo đảm việc gửi báo cáo tới Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc đúng thời hạn:
- Báo cáo phản ứng có hại nghiêm trọng gây tử vong hoặc đe dọa tính mạng người bệnh: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 7 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại nghiêm trọng còn lại: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 15 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại không nghiêm trọng có thể tập hợp gửi hàng tháng, trước ngày mùng 5 của tháng kế tiếp.
d) Báo cáo từ khoa/phòng lâm sàng tới khoa Dược hoặc đơn vị đầu mối được phân công tập hợp báo cáo ADR tại cơ sở khám bệnh, chữa bệnh cần được gửi trong thời gian sớm nhất có thể sau khi xảy ra phản ứng. Thời hạn gửi theo quy định tại cơ sở khám bệnh, chữa bệnh, tùy thuộc vào tình hình thực tế nhưng không quá thời hạn gửi báo cáo tới Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
3.4.3. Thời gian gửi báo cáo
a) Báo cáo cần được gửi trong thời gian sớm nhất có thể sau khi phát hiện ra phản ứng, ngay cả khi thông tin thu được chưa đầy đủ (báo cáo ban đầu). Trong trường hợp này, có thể bổ sung báo cáo nếu thu thập được thêm thông tin (báo cáo bổ sung). b) Báo cáo trong khi người bệnh chưa xuất viện giúp khai thác đủ thông tin, thực hiện các xét nghiệm cần thiết để xác định nguyên nhân gây ADR. c) Bảo đảm việc gửi báo cáo tới Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc đúng thời hạn:
- Báo cáo phản ứng có hại nghiêm trọng gây tử vong hoặc đe dọa tính mạng người bệnh: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 7 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại nghiêm trọng còn lại: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 15 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại không nghiêm trọng có thể tập hợp gửi hàng tháng, trước ngày mùng 5 của tháng kế tiếp.
d) Báo cáo từ khoa/phòng lâm sàng tới khoa Dược hoặc đơn vị đầu mối được phân công tập hợp báo cáo ADR tại cơ sở khám bệnh, chữa bệnh cần được gửi trong thời gian sớm nhất có thể sau khi xảy ra phản ứng. Thời hạn gửi theo quy định tại cơ sở khám bệnh, chữa bệnh, tùy thuộc vào tình hình thực tế nhưng không quá thời hạn gửi báo cáo tới Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
3.4.3. Thời gian gửi báo cáo
a) Báo cáo cần được gửi trong thời gian sớm nhất có thể sau khi phát hiện ra phản ứng, ngay cả khi thông tin thu được chưa đầy đủ (báo cáo ban đầu). Trong trường hợp này, có thể bổ sung báo cáo nếu thu thập được thêm thông tin (báo cáo bổ sung). b) Báo cáo trong khi người bệnh chưa xuất viện giúp khai thác đủ thông tin, thực hiện các xét nghiệm cần thiết để xác định nguyên nhân gây ADR. c) Bảo đảm việc gửi báo cáo tới Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc đúng thời hạn:
- Báo cáo phản ứng có hại nghiêm trọng gây tử vong hoặc đe dọa tính mạng người bệnh: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 7 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại nghiêm trọng còn lại: gửi trong thời gian sớm nhất có thể nhưng không muộn hơn 15 ngày làm việc kể từ thời điểm phát hiện ra phản ứng.
- Báo cáo phản ứng có hại không nghiêm trọng có thể tập hợp gửi hàng tháng, trước ngày mùng 5 của tháng kế tiếp.
d) Báo cáo từ khoa/phòng lâm sàng tới khoa Dược hoặc đơn vị đầu mối được phân công tập hợp báo cáo ADR tại cơ sở khám bệnh, chữa bệnh cần được gửi trong thời gian sớm nhất có thể sau khi xảy ra phản ứng. Thời hạn gửi theo quy định tại cơ sở khám bệnh, chữa bệnh, tùy thuộc vào tình hình thực tế nhưng không quá thời hạn gửi báo cáo tới Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
3.4.4. Hướng dẫn điền mẫu báo cáo phản ứng có hại của thuốc
a) Nguyên tắc chung - Hoàn thành mẫu báo cáo với đầy đủ thông tin nhất có được từ bệnh án.
- Sử dụng một bản báo cáo riêng cho mỗi người bệnh.
- Trường hợp dùng thuốc để điều trị ADR nhưng lại gây ra một ADR khác cho người bệnh nên tách thành một báo cáo riêng.
- Chữ viết rõ ràng, viết chính xác tên thuốc, hạn chế viết tắt.
- Điền thông tin chính xác, thống nhất, tránh mâu thuẫn giữa các thông tin trong báo cáo.
- Khuyến khích áp dụng công nghệ thông tin trong báo cáo ADR.
b) Mẫu báo cáo ADR Mẫu báo cáo ADR được ban hành kèm theo Thông tư số 23/2011/TTBYT ngày 10 tháng 6 năm 2011 về Hướng dẫn sử dụng thuốc trong các cơ sở y tế có giường bệnh (xem Phụ lục 3). Đối với các hoạt động phát hiện ADR thông qua giám sát tích cực, có thể sử dụng mẫu báo cáo đã xây dựng riêng trong hoạt động đó, tuy nhiên vẫn phải đảm bảo có đầy đủ các thông tin tối thiểu cần điền được liệt kê trong mục 3.4.4.c của Hướng dẫn này.
c) Các thông tin tối thiểu cần điền trong mẫu báo cáo ADR - Thông tin về người bệnh: họ và tên, tuổi hoặc ngày sinh, giới tính. - Thông tin về phản ứng có hại: mô tả chi tiết biểu hiện ADR, ngày xuất hiện phản ứng, diễn biến ADR sau khi xử trí (bao gồm diễn biến sau khi ngừng thuốc hoặc giảm liều thuốc hoặc tái sử dụng thuốc nghi ngờ). - Thông tin về thuốc nghi ngờ: tên thuốc nghi ngờ, liều dùng, đường dùng, lý do sử dụng thuốc, ngày và thời điểm bắt đầu dùng thuốc. - Thông tin về người và đơn vị báo cáo: tên đơn vị báo cáo, họ và tên người báo cáo, chức vụ, số điện thoại liên lạc hoặc địa chỉ email (nếu có). - Với các thông tin còn lại trong mẫu báo cáo, khuyến khích nhân viên y tế thu thập, bổ sung tối đa thông tin.
d) Hướng dẫn chi tiết các thông tin cần điền trong báo cáo ADR - Thông tin hành chính
- Nơi báo cáo: Ghi tên khoa/phòng điều trị, tên cơ sở khám bệnh, chữa bệnh hay nơi phát hiện phản ứng và tên tỉnh/thành phố.
- Mã số báo cáo của đơn vị: do cơ sở khám bệnh, chữa bệnh tự quy định để thuận tiện cho việc theo dõi và quản lý báo cáo ADR. Đơn vị cũng có thể sử dụng mã số bệnh án của người bệnh để thay thế mã số báo cáo này.
- Mã số báo cáo (do Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc quản lý): phần này do Trung tâm Quốc gia hoặc Trung tâm khu vực điền sau khi nhận được báo cáo.
- Thông tin về người bệnh
- Mục 1: điền họ và tên của người bệnh.
- Mục 2: điền thông tin tuổi của người bệnh theo một trong hai cách sau: • Cách 1: Ngày sinh: điền ngày/tháng/năm sinh của người bệnh hoặc chỉ điền “Năm sinh” trong trường hợp không rõ ngày, tháng. • Cách 2: Tuổi: điền tuổi của người bệnh cho tới thời điểm xảy ra ADR. Trường hợp bệnh nhi dưới 1 tuổi và bệnh nhi sơ sinh: cần ghi rõ tháng tuổi hoặc ngày tuổi. + Mục 3: đánh dấu (√) vào một trong hai ô lựa chọn Nam hoặc Nữ. + Mục 4: điền cân nặng của người bệnh (nếu có thông tin).
- Thông tin về phản ứng có hại
- + Mục 5: điền thông tin thời điểm bắt đầu xuất hiện phản ứng có hại trên người bệnh theo ngày/tháng/năm.
- + Mục 6: điền khoảng thời gian từ thời điểm lần dùng cuối cùng của thuốc nghi ngờ gây ADR tới thời điểm xuất hiện phản ứng có hại.
- + Mục 7: mô tả biểu hiện ADR. Chú ý mô tả rõ các dấu hiệu, triệu chứng bất thường cụ thể xuất hiện trên người bệnh, diễn biến lâm sàng của các triệu chứng bất thường này, đặc biệt khi giảm liều/ngừng sử dụng hay tái sử dụng thuốc nghi ngờ gây phản ứng. Không ghi chung chung như: phản ứng dịch truyền, dị ứng...
- + Mục 8: điền kết quả các xét nghiệm cận lâm sàng, đặc biệt lưu ý các kết quả xét nghiệm bất thường có liên quan đến phản ứng và diễn biến của các kết quả này trong quá trình xử trí ADR.
Ghi chú: Mục 7 và mục 8 nên được nhân viên y tế trực tiếp chăm sóc và điều trị người bệnh điền hoặc kiểm tra lại thông tin nếu thông tin được điền bởi các nhân viên y tế khác.
- + Mục 9: điền thông tin về tiền sử của người bệnh (nếu khai thác được thông tin) bao gồm: tiền sử xảy ra ADR (người bệnh đã từng gặp phản ứng có hại tương tự trước đó với thuốc nghi ngờ gây ADR hoặc các thuốc cùng nhóm hay chưa?), tiền sử dị ứng, tình trạng thai nghén, nghiện thuốc lá, nghiện rượu, bệnh lý gan, thận (nếu có) của người bệnh.
- + Mục 10: điền thông tin các biện pháp đã thực hiện để xử trí phản ứng bao gồm: biện pháp xử trí, thuốc điều trị triệu chứng, thuốc điều trị hỗ trợ và các biện pháp đảm bảo chức năng sống cho người bệnh.
- + Mục 11: đánh dấu (√) vào một hoặc nhiều ô thể hiện mức độ nghiêm trọng của phản ứng có hại (theo nhận định của người báo cáo) bao gồm: tử vong, đe dọa tính mạng, nhập viện/kéo dài thời gian nằm viện, tàn tật vĩnh viễn/nặng nề, dị tật thai nhi. Trường hợp người báo cáo nhận định phản ứng ở mức độ nhẹ, đánh dấu vào ô “Không nghiêm trọng”.
- + Mục 12: đánh dấu (√) vào một trong các ô tương ứng thể hiện kết quả sau khi xử trí ADR bao gồm: tử vong do ADR, tử vong không liên quan đến thuốc, chưa hồi phục, đang hồi phục, hồi phục có di chứng, hồi phục không để lại di chứng.
- Thông tin về thuốc nghi ngờ gây ADR
- + Mục 13: Thông tin về thuốc nghi ngờ gây ADR • Ghi rõ ràng, đầy đủ các mục yêu cầu bao gồm: tên thuốc, liều dùng, đường dùng, lý do sử dụng thuốc cho người bệnh, ngày và thời gian bắt đầu dùng thuốc, ngày và thời gian kết thúc dùng thuốc; nhà sản xuất, số lô. Chú ý: không nhầm lẫn giữa “lý do sử dụng thuốc” và “biểu hiện ADR”. • Mẫu báo cáo để khoảng trống để ghi tối đa 4 thuốc nghi ngờ gây ra phản ứng. Nếu số lượng thuốc nghi ngờ nhiều hơn, người báo cáo có thể gửi kèm một bản chú thích bổ sung. Tên thuốc nên được ghi bằng cả tên biệt dược và tên chung quốc tế (INN).
- + Mục 14: diễn biến ADR sau khi ngừng thuốc hoặc giảm liều thuốc nghi ngờ (đánh dấu (√) vào từng dòng theo thứ tự tương ứng với thuốc nghi ngờ được liệt kê ở mục số 13). • Trường hợp vẫn duy trì sử dụng thuốc nghi ngờ: đánh dấu (√) vào ô “Không ngừng/giảm liều”. • Trường hợp ngừng thuốc hoặc giảm liều thuốc: đánh dấu (√) vào một trong hai lựa chọn “ Có/ Không” để xác định ADR có cải thiện sau khi ngừng thuốc hoặc giảm liều hay không. • Trường hợp không có thông tin về diễn biến ADR sau khi ngừng thuốc hoặc giảm liều thuốc nghi ngờ thì đánh dấu (√) vào ô “Không có thông tin”.
- + Mục 15: diễn biến ADR sau khi tái sử dụng lại thuốc nghi ngờ (đánh dấu (√) vào từng dòng theo thứ tự tương ứng với thuốc nghi ngờ được liệt kê ở mục số 13). • Trường hợp không tái sử dụng lại thuốc nghi ngờ: đánh dấu (√) vào ô “Không tái sử dụng”. • Trường hợp tái sử dụng lại thuốc nghi ngờ: đánh dấu (√) vào một trong hai lựa chọn “ Có/ Không” để xác định ADR có xuất hiện lại sau khi tái sử dụng thuốc hay không. • Trường hợp không có thông tin về diễn biến ADR sau khi tái sử dụng lại thuốc nghi ngờ thì đánh dấu (√) vào ô “Không có thông tin” Chú ý: Cần thận trọng khi tái sử dụng thuốc nghi ngờ. Chỉ sử dụng lại thuốc nghi ngờ gây ADR khi không có thuốc điều trị thay thế hoặc khi lợi ích của thuốc vượt trội hơn so với nguy cơ, đồng thời đảm bảo được các biện pháp cần thiết xử trí ADR.
- + Mục 16: liệt kê các thuốc dùng đồng thời với các thuốc nghi ngờ (không ghi các thuốc sử dụng để điều trị phản ứng có hại trong mục này) theo các mục yêu cầu: tên thuốc, thời gian bắt đầu và kết thúc sử dụng các thuốc đó. Nên ghi rõ đường dùng và liều dùng của các thuốc này.
- Phần đánh giá ADR của đơn vị
- + Mục 17, 18: việc đánh giá mối liên quan giữa thuốc và ADR là không bắt buộc, được thực hiện tùy thuộc điều kiện chuyên môn của từng bệnh viện. Đánh giá mối liên quan giữa thuốc và ADR có thể được thực hiện theo thang phân loại của Tổ chức Y tế thế giới hoặc theo thang điểm Naranjo (xem Phụ lục 7).
- + Mục 19: người báo cáo có thể đưa ra ý kiến chuyên môn liên quan đến ADR và bệnh nhân trong báo cáo dựa trên thực tế lâm sàng ghi nhận, đánh giá và xử trí ADR.
- Thông tin về người báo cáo
- + Mục 20: điền đầy đủ các thông tin cá nhân bao gồm: Họ và tên, chức danh/chức vụ, điện thoại liên lạc hoặc địa chỉ, email (nếu có). Thông tin về người báo cáo sẽ được bảo mật. Các thông tin này giúp Trung tâm Thông tin thuốc và Theo dõi phản ứng có hại của thuốc liên hệ trong trường hợp cần thiết và để phản hồi thông tin thẩm định cho người báo cáo.
- + Mục 21: người báo cáo ký xác nhận.
- + Mục 22: khi có thêm thông tin bổ sung cho một ca báo cáo ADR đã gửi đi trước đó, người báo cáo nên điền vào một bản báo cáo ADR mới và ghi chú bằng cách đánh dấu (√) thích hợp vào nội dung số 22 (Dạng báo cáo: Lần đầu/Bổ sung) trên mẫu báo cáo. Người báo cáo có thể ghi thêm chú thích trên bản báo cáo bổ sung hoặc thông báo qua điện thoại, fax, hoặc email cho Trung tâm về ngày báo cáo hoặc mã số của báo cáo lần đầu tương ứng.
- + Mục 23: điền ngày/tháng/năm làm báo cáo báo cáo.
3.4.5. Hình thức gửi báo cáo ADR
a) Với các cơ sở khám bệnh, chữa bệnh có Khoa Dược Nhân viên y tế gửi báo cáo ADR tới Khoa Dược là đầu mối tập hợp báo cáo trong bệnh viện. Trong trường hợp cần thiết, có thể gửi báo cáo trực tiếp đến Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc hoặc các Trung tâm khu vực, sau đó thông báo lại cho khoa Dược.
b) Với các cơ sở khám bệnh, chữa bệnh không tổ chức Khoa Dược Nhân viên y tế gửi báo cáo đến bộ phận Dược lâm sàng là đầu mối tập hợp báo cáo tại đơn vị hoặc có thể gửi trực tiếp đến Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc hoặc các Trung tâm khu vực.
c) Báo cáo ADR được điền vào mẫu báo cáo theo quy định và gửi về Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc Bằng một trong 4 hình thức sau:
- Cách 1: Gửi qua bưu điện.
- Cách 2: Gửi qua thư điện tử (email).
- Cách 3: Báo cáo ADR trực tuyến + Truy cập vào trang web: http://canhgiacduoc.org.vn. + Đọc và làm theo hướng dẫn trên trang web.
- Cách 4: Điện thoại báo cáo trực tiếp cho Trung tâm trong trường hợp khẩn cấp. Thông tin sau đó cần được điền vào mẫu báo cáo và gửi về Trung tâm theo một trong ba cách nêu trên.
3.4.6. Nơi nhận báo cáo Báo cáo có thể gửi về một trong hai địa chỉ sau:
a) Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc (nhận báo cáo từ tất cả các tỉnh/thành phố trên phạm vi toàn quốc) Địa chỉ: Trường Đại học Dược Hà Nội, 13-15 Lê Thánh Tông, Quận Hoàn Kiếm, Hà Nội. Điện thoại: (024) 3933 5618 E-mail: di.pvcenter@gmail.com Trang thông tin điện tử: http://canhgiacduoc.org.vn
b) Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc thành phố Hồ Chí Minh (nhận báo cáo của các tỉnh/thành phố từ Đà Nẵng trở vào) Địa chỉ: Bệnh viện Chợ Rẫy, 201B Nguyễn Chí Thanh, Phường 12, Quận 5, Thành phố Hồ Chí Minh. Điện thoại: (028) 3855 4137- Ext: 794 hoặc (028) 3856 3537 E-mail: adrhcm@choray.vn
3.4.7. Phản hồi báo cáo từ phía Trung tâm Quốc gia và các Trung tâm Khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc
- Khi nhận được báo cáo ADR, Trung tâm Quốc gia hoặc Trung tâm khu vực sẽ gửi thư xác nhận cảm ơn tới đơn vị/cá nhân đã gửi báo cáo. - Các báo cáo ADR sẽ được Trung tâm Quốc gia hoặc Trung tâm khu vực thẩm định theo Quy trình xử lý báo cáo ADR của Trung tâm. - Định kỳ hàng năm, Trung tâm Quốc gia tổ chức tổng kết, phân loại báo cáo ADR, gửi báo cáo tổng kết công tác báo cáo ADR về Bộ Y tế, Y tế Ngành, các Sở Y tế và các cơ sở khám bệnh, chữa bệnh. - Trong trường hợp cần phản hồi nhanh, đặc biệt với các ADR nghiêm trọng, Trung tâm Quốc gia hoặc Trung tâm khu vực sẽ nhanh chóng tiến hành thu thập thông tin và thẩm định để gửi phản hồi cho nhân viên y tế, cơ sở khám bệnh, chữa bệnh đã gửi báo cáo.
3.5. Đánh giá ADR
Trước khi quy kết biến cố bất lợi xảy ra có liên quan đến thuốc không, các hoạt động đánh giá sẽ dựa trên thông tin của biến cố bất lợi ghi nhận được. Khái niệm biến cố bất lợi được dùng thay cho ADR.
3.5.1. Đánh giá mức độ nghiêm trọng
Thông tin về mức độ nghiêm trọng của biến cố bất lợi phản ánh hậu quả gây ra trên người bệnh. Một biến cố bất lợi được đánh giá là nghiêm trọng (serious adverse event - SAE) nếu biến cố bất lợi đó xảy ra và dẫn đến một trong những hậu quả sau đây:
- Tử vong.
- Đe dọa tính mạng.
- Để lại di chứng.
- Người bệnh cần phải nhập viện.
- Kéo dài thời gian nằm viện.
- Gây dị tật bẩm sinh ở thai nhi.
- Các hậu quả khác được nhân viên y tế đánh giá là nghiêm trọng có ý nghĩa lâm sàng.
3.5.2. Đánh giá mức độ nặng
Việc đánh giá mức độ nặng của biến cố bất lợi sẽ giúp nhân viên y tế nhanh chóng đưa ra biện pháp xử trí, can thiệp phù hợp. Để đánh giá mức độ nặng của biến cố bất lợi có thể áp dụng thang phân loại của Viện Ung thư Quốc gia Hoa Kỳ (CTCAE), mức độ nặng của biến cố bất lợi được phân loại thành 5 mức độ như sau:
- Mức độ 1 (nhẹ): Không có triệu chứng hoặc triệu chứng nhẹ; chỉ biết được thông qua quan sát để chẩn đoán hoặc biểu hiện lâm sàng; không cần đến can thiệp.
- Mức độ 2 (trung bình): Cần đến can thiệp tối thiểu, tại chỗ hoặc không xâm lấn; ảnh hưởng đến một số chức năng vận động hoặc sinh hoạt thông thường.
- Mức độ 3 (nặng): Ảnh hưởng đáng kể trên lâm sàng nhưng chưa đến mức đe dọa tính mạng; khiến người bệnh phải nhập viện hoặc kéo dài thời gian nằm viện; bị dị tật; giới hạn khả năng tự chăm sóc bản thân của người bệnh.
- Mức độ 4 (đe dọa tính mạng): Gây ra hậu quả đe dọa tính mạng người bệnh; cần can thiệp khẩn cấp.
- Mức độ 5 (tử vong): Tử vong liên quan đến biến cố bất lợi.
3.5.3. Đánh giá mối quan hệ nhân quả
a) Việc đánh giá mối quan hệ nhân quả giữa biến cố bất lợi và thuốc nghi ngờ giúp nhân viên y tế xác định biện pháp xử trí và dự phòng phù hợp. Khi nghi ngờ một biến cố bất lợi do thuốc, cần đánh giá chi tiết biến cố bất lợi đó dựa trên các yếu tố liên quan đến thuốc và người bệnh cụ thể:
- Các yếu tố liên quan đến người bệnh bao gồm tuổi, giới tính, cân nặng, bệnh chính và các bệnh mắc kèm trước khi ghi nhận phản ứng nghi ngờ do thuốc.
- Các yếu tố liên quan đến thuốc bao gồm các thuốc nghi ngờ gây biến cố bất lợi (tên thuốc, liều dùng, đường dùng, nhà sản xuất, số lô, thời gian bắt đầu dùng thuốc và thời gian ngừng thuốc, chỉ định) và các thuốc khác đã được người bệnh sử dụng trước thời điểm xảy ra biến cố, chú ý cả các thuốc không kê đơn, thuốc đã ngừng sử dụng trong thời gian gần đây, các thuốc bổ sung hoặc thay thế.
- Thông tin chi tiết về biến cố bất lợi bao gồm mô tả phản ứng, thời gian khởi phát và khoảng thời gian xảy ra phản ứng, hậu quả của phản ứng, xử trí và kết quả sau xử trí, kết quả xét nghiệm có liên quan.
b) Khi đánh giá mối quan hệ nhân quả giữa thuốc nghi ngờ và biến cố bất lợi, cần tra cứu xem biến cố bất lợi đã được ghi nhận trong các tài liệu thông tin thuốc bao gồm tờ hướng dẫn sử dụng và các tài liệu tra cứu y văn về thuốc khác. Tùy theo điều kiện chuyên môn, có thể đánh giá mối liên hệ giữa thuốc nghi ngờ và biến cố bất lợi xuất hiện trên người bệnh theo thang phân loại của Tổ chức Y tế Thế giới hoặc thang điểm của Naranjo (xem Phụ lục 7). Đây là hai thang quy kết được sử dụng rộng rãi hiện nay.
- Đánh giá mối quan hệ nhân quả theo thang của Tổ chức Y tế thế giới (WHO): Thang quy kết mối quan hệ nhân quả của WHO đã được thẩm định và áp dụng phổ biến trong thực hành để đánh giá các báo cáo phản ứng có hại của thuốc. Phương pháp này dựa trên những xem xét về mặt dược lý – lâm sàng của ca bệnh và chất lượng thông tin báo cáo. Dựa trên một số tiêu chuẩn đánh giá, mối quan hệ nhân quả được chia thành 6 mức là “chắc chắn”, “có khả năng”, “có thể”, “không chắc chắn”, “chưa phân loại” và “không thể phân loại”. Mặc dù, còn có hạn chế phụ thuộc vào chủ quan của người đánh giá và có tính chất định tính nhưng phương pháp này vẫn được coi là phương pháp đơn giản, dễ áp dụng trong nhiều trường hợp.
- Đánh giá mối quan hệ nhân quả theo thang Naranjo: Thang Naranjo là một thang quy kết ADR bao gồm 10 câu hỏi với câu trả lời là “có”, “không” và “không biết” để đánh giá nhân quả trong nhiều tình huống lâm sàng khác nhau. Điểm số có được từ mỗi câu hỏi thay đổi từ -1 đến +2. Biến cố được quy kết theo 4 mức “chắc chắn” (9), “có khả năng” (5-8), “có thể” (1-4) và nghi ngờ (0). Đây là một thang đánh giá ADR sử dụng thuật toán ít phức tạp và tốn ít thời gian. Tuy nhiên, các câu hỏi từ 6 đến 10 thường khó có thông tin để trả lời.
3.5.4. Đánh giá khả năng phòng tránh được của ADR
Các ADR “phòng tránh được” phản ánh các vấn đề liên quan đến thuốc có thể gây tổn thương thực sự trên người bệnh. Do đó, nhân viên y tế (đặc biệt là các dược sĩ lâm sàng) cần được trang bị các kỹ năng cần thiết và được đào tạo phù hợp nhằm phát hiện các ADR phòng tránh được để phát hiện các vấn đề tiềm tàng liên quan đến thuốc.
a) Phương pháp đánh giá
Tuỳ theo đặc thù chuyên môn của từng cơ sở khám bệnh, chữa bệnh, có thể đánh giá khả năng phòng tránh được của ADR theo phương pháp P (được đề xuất bởi nhóm chuyên gia của WHO) hoặc phương pháp của mạng lưới các Trung tâm Cảnh giác Dược Pháp.
* Phương pháp P đề xuất bởi nhóm chuyên gia của WHO - Phương pháp P cho phép khám phá toàn bộ quy trình sử dụng thuốc từ kê đơn cho đến theo dõi, giám sát người bệnh trong quá trình sử dụng thuốc, nhằm xác định các yếu tố nguy cơ có thể phòng tránh được liên quan đến khả năng xuất hiện ADR. Các yếu tố nguy cơ này được xếp loại trong bộ 20 tiêu chí đánh giá khả năng phòng tránh được của ADR, bao gồm yếu tố nguy cơ liên quan đến thực hành của nhân viên y tế (tiêu chí 1 đến tiêu chí 16), hành vi của người bệnh (tiêu chí 19 và 20) và chất lượng thuốc (tiêu chí 5, 6, 17 và 18) (xem Phụ lục 8).
- Kết quả đánh giá sẽ rơi vào 1 trong 3 trường hợp: "có thể phòng tránh được", "không thể phòng tránh được" và "không đánh giá được".
- Khuyến khích sử dụng tờ hướng dẫn sử dụng thuốc, các hướng dẫn điều trị của Bộ Y tế, của các hiệp hội chuyên môn trong nước và trên thế giới, và các tài liệu tham chiếu tương tự khi đánh giá khả năng phòng tránh được của ADR.
* Phương pháp của mạng lưới các Trung tâm Cảnh giác Dược Pháp Với phương pháp này, khả năng phòng tránh được của ADR được đánh giá bằng cách chọn câu trả lời và cho điểm cho từng mục theo các câu hỏi trong bộ tiêu chí (xem Phụ lục 8). Các tiêu chí đánh giá được phân loại theo hai mục, lần lượt là:
- Phát hiện các sai sót trong quy trình sử dụng thuốc (sai sót trong quá trình sản xuất, cấp phát, kê đơn, sử dụng, dịch đơn, tự ý sử dụng thuốc kê đơn và vấn đề trong tuân thủ);
- Đánh giá tính phù hợp của việc sử dụng thuốc trên người bệnh (phù hợp với khuyến cáo, các yếu tố nguy cơ, hoàn cảnh sống và tình trạng bệnh lý của người bệnh). Mỗi phương án trả lời sẽ được quy đổi thành điểm số.
- Khả năng phòng tránh được của ADR được phân loại theo 4 mức độ dựa trên sai sót phát hiện được hoặc điểm tổng của từng thuốc nghi ngờ được đánh giá, gồm có: “phòng tránh được” (-13 đến -8), “có khả năng phòng tránh được” (-7 đến -3), “không đánh giá được” (-2 đến 2) và “không phòng tránh được” (+3 đến +8).
b) Phân loại nguyên nhân gây ra ADR phòng tránh được
* Nguyên nhân liên quan chất lượng thuốc Trường hợp nghi ngờ nguyên nhân liên quan đến chất lượng thuốc hoặc nếu phản ứng có hại xảy ra liên tục với một thuốc hoặc một lô thuốc trong thời gian ngắn tại cơ sở khám bệnh, chữa bệnh, nhân viên y tế cần:
- Kiểm tra chất lượng cảm quan mẫu thuốc được lưu lại xem có biểu hiện gì về chất lượng thuốc.
- Xác định tỷ lệ người bệnh gặp biến cố trên tổng số người bệnh đã dùng thuốc đó, so sánh với tỷ lệ y văn. Nếu tỷ lệ ghi nhận cao hơn y văn, nên liên hệ lấy mẫu để kiểm nghiệm.
- Việc lấy mẫu thuốc để kiểm nghiệm thực hiện theo quy định tại Phụ lục I, biên bản lấy mẫu theo quy định tại Mẫu số 1 Phụ lục III ban hành theo Thông tư số 11/2018/TT-BYT ngày 04 tháng 5 năm 2018 của Bộ trưởng Bộ Y tế quy định về chất lượng thuốc, nguyên liệu làm thuốc. Trường hợp thuốc không đạt tiêu chuẩn chất lượng, xử lý theo khoản 11 Điều 1 Thông tư số 03/2020/TT-BYT ngày 22 tháng 01 năm 2020 của Bộ trưởng Bộ Y tế sửa đổi, bổ sung một số điều của Thông tư số 11/2018/TT-BYT ngày 04 tháng 5 năm 2018 của Bộ trưởng Bộ Y tế.
- Gửi báo cáo cho Trung tâm DI&ADR Quốc gia hoặc Khu vực theo hướng dẫn tại mục 3.4 của Hướng dẫn này.
* Nguyên nhân liên quan đến sai sót trong quá trình sử dụng thuốc - Khi nghi ngờ có sai sót xảy ra trong quá trình sử dụng thuốc, dược sĩ lâm sàng thu thập thông tin và giúp Hội đồng Thuốc và điều trị của cơ sở khám bệnh, chữa bệnh tổ chức hội chẩn, thảo luận và đánh giá để đi đến kết luận cho hướng xử trí và đề xuất các biện pháp dự phòng tiếp theo. - Việc phân loại hậu quả những sai sót liên quan đến thuốc xem Phụ lục 6 của Hướng dẫn này. - Những thông tin về sai sót cũng cần được thông báo hoặc tập huấn để rút kinh nghiệm trong cơ sở, đồng thời, có thể cần cập nhật, bổ sung, sửa đổi danh mục thuốc, hướng dẫn điều trị và các quy trình chuyên môn khác tại cơ sở để phòng tránh các sai sót.
3.5.5. Tổng kết dữ liệu ADR định kỳ
Việc tổng kết định kỳ các báo cáo ADR (đặc biệt là báo cáo ADR nghiêm trọng và ADR phòng tránh được), báo cáo sai sót liên quan đến thuốc và báo cáo chất lượng thuốc giúp cơ sở khám bệnh, chữa bệnh có thể định hướng được các biện pháp can thiệp phù hợp, đảm bảo việc sử dụng thuốc hợp lý, an toàn và hiệu quả. Các chỉ tiêu tổng kết có thể bao gồm:
- Số lượng báo cáo, phân loại báo cáo theo Khoa/phòng điều trị.
- Số lượng báo cáo đã gửi tới các Trung tâm DI&ADR.
- Phân loại thuốc nghi ngờ gây biến cố theo nhóm tác dụng dược lý.
- Phân loại biến cố được ghi nhận theo mức độ nghiêm trọng, theo khả năng phòng tránh được và theo tổ chức cơ thể bị ảnh hưởng.
- Các cặp thuốc – biến cố đặc biệt cần lưu ý.
- Đánh giá chất lượng báo cáo theo thang điểm VigiGrade (xem Phụ lục 9).
- Phân tích xu hướng ADR liên quan đến thuốc theo nguyên lý Pareto (nguyên lý 80/20) để xác định tín hiệu an toàn thuốc cần đánh giá chi tiết hơn.
- Phân tích xu hướng tỷ lệ ADR cụ thể của một thuốc được xác định là tín hiệu cần đánh giá chi tiết hơn theo thời gian (hàng tháng), so sánh tỷ lệ này với tỷ lệ được ghi nhận trong y văn và tỷ lệ ghi nhận ADR trung bình tại cơ sở khám bệnh, chữa bệnh.
3.6. Dự phòng ADR
- Nhiều phản ứng có hại của thuốc có thể ngăn ngừa được bằng các biện pháp dự phòng trong quá trình sử dụng thuốc cho người bệnh. Để dự phòng ADR, trước hết các đối tác tham gia hoạt động giám sát ADR trong cơ sở khám bệnh, chữa bệnh cần tổ chức thực hiện hoạt động giám sát ADR theo Phần IV của Hướng dẫn này. - Bên cạnh đó, theo chu trình của hoạt động giám sát ADR trong cơ sở khám bệnh, chữa bệnh, sau khi đánh giá ADR, khoa Dược (hoặc bộ phận Dược lâm sàng), phòng Kế hoạch tổng hợp, phòng Quản lý chất lượng hoặc đơn vị đầu mối được phân công cần tư vấn cho Hội đồng Thuốc và điều trị và người đứng đầu cơ sở khám bệnh, chữa bệnh phê duyệt và triển khai kế hoạch giám sát và giảm thiểu ADR để giúp hạn chế xuất hiện lại các ADR có thể phòng tránh được.
3.6.1. Xây dựng và triển khai kế hoạch giám sát và giảm thiểu ADR
3.6.1.1. Nguyên tắc chung
- Xây dựng và triển khai kế hoạch giám sát và giảm thiểu phản ứng có hại của một thuốc là trọng tâm của hoạt động dự phòng ADR đối với thuốc đó. Để tối ưu hiệu quả của hoạt động dự phòng ADR nên lưu ý tập trung vào các ADR quan trọng với các đặc điểm sau:
- ADR tái xuất hiện, có khả năng xảy ra với một người bệnh khác nếu không được can thiệp.
- ADR dễ phát hiện, được xác định rõ ràng và không quy kết được cho các nguyên nhân có thể khác.
- ADR có thể phòng tránh được thông qua các biện pháp can thiệp phù hợp. Các ADR quan trọng này có thể phòng tránh được thông qua việc triển khai các giải pháp ngăn chặn các sai sót có khả năng xảy ra, phát hiện sai sót và giảm thiểu hậu quả do sai sót. Mục tiêu chính là xây dựng lại quy trình quản lý thuốc để tránh xảy ra sai sót tương tự.
- Kế hoạch giảm thiểu ADR cần có nội dung triển khai các can thiệp giúp giảm thiểu ADR để giảm mức độ nặng và mức độ thường gặp của ADR trên người bệnh, đặc biệt đối với các ADR được xác định quan trọng. Kế hoạch giảm thiểu ADR gồm hai nhóm hoạt động chính:
- Các can thiệp giảm thiểu ADR thường quy (xây dựng hệ thống các danh mục thuốc cần lưu ý, thông tin thuốc cho nhân viên y tế và người bệnh).
- Các can thiệp giảm thiểu ADR tăng cường (quản lý thuốc có nguy cơ cao, quản lý người bệnh có nguy cơ cao, đào tạo tập huấn cho nhân viên y tế, đánh giá sử dụng thuốc, cập nhật sửa đổi hướng dẫn sử dụng thuốc…).
3.6.1.2. Một số hoạt động giám sát và giảm thiểu ADR cần lưu ý triển khai tại cơ sở khám bệnh, chữa bệnh
a) Xây dựng hệ thống các danh mục thuốc cần lưu ý Để giảm thiểu nguy cơ xuất hiện ADR, cơ sở khám bệnh, chữa bệnh cần xây dựng các danh mục thuốc cần lưu ý sau:
- Danh mục thuốc nhìn giống nhau, đọc giống nhau (LASA).
- Danh mục thuốc không nhai, nghiền, bẻ.
- Danh mục tương tác thuốc.
- Danh mục tương hợp, tương kỵ.
- Danh mục thuốc cần hiệu chỉnh liều.
- Danh mục cách pha, bảo quản và sử dụng các thuốc dùng đường tiêm truyền.
- Danh mục khác giúp giảm thiểu ADR.
b) Quản lý các thuốc có nguy cơ cao
Cơ sở khám bệnh, chữa bệnh cần xây dựng chương trình quản lý các thuốc có nguy cơ cao bao gồm các hệ thống quản lý việc sử dụng thuốc phù hợp với chính sách y tế về quản lý thuốc tại cơ sở. Chương trình quản lý thuốc có nguy cơ cao cần bao gồm các yếu tố tối thiểu sau:
* Danh mục thuốc có nguy cơ cao và hướng dẫn quản lý thuốc có quy cơ cao - Danh mục thuốc có nguy cơ cao là danh sách các thuốc hoặc nhóm thuốc có nguy cơ cao gây rủi ro được sử dụng tại cơ sở khám bệnh, chữa bệnh. Phụ lục 11 liệt kê các thuốc nhóm thuốc cần xem xét đưa vào danh mục thuốc có nguy cơ cao. Phụ lục này có thể chưa liệt kê đầy đủ các thuốc có nguy cơ cao. Do đó, mỗi cơ sở khám bệnh, chữa bệnh nên xây dựng danh mục các thuốc hoặc nhóm thuốc có nguy cơ cao và hướng dẫn quản lý các thuốc có nguy cơ cao phù hợp với loại thuốc được sử dụng và đối tượng người bệnh được điều trị tại đơn vị (xem Phụ lục 12). - Cơ sở khám bệnh, chữa bệnh cần có kế hoạch xây dựng, cập nhật danh mục thuốc có nguy cơ cao, và hướng dẫn quản lý sử dụng thuốc tại đơn vị. Trước khi đưa một thuốc vào danh mục thuốc có nguy cơ cao, cần rà soát khả năng gặp sai sót liên quan tới thuốc đó trong y văn. Nếu xác định được việc vô tình sử dụng thuốc, lạm dụng thuốc, kê đơn hoặc thực hiện thuốc không phù hợp có thể dẫn đến nguy cơ cao gặp phản ứng có hại nghiêm trọng hoặc đe doạ tính mạng, thì cần đưa vào danh mục và có hướng dẫn quản lý sử dụng phù hợp. - Việc xây dựng Hướng dẫn quản lý thuốc có nguy cơ cao cần có sự tham gia tư vấn của các chuyên gia trong lĩnh vực chuyên môn liên quan và phù hợp với chính sách quản lý thuốc tại cơ sở khám bệnh, chữa bệnh, đồng thời được Hội đồng Thuốc và điều trị hoặc người đứng đầu cơ sở khám bệnh, chữa bệnh phê duyệt. Nội dung hướng dẫn có thể bao gồm:
- Yêu cầu khi kê đơn và sử dụng thuốc có nguy cơ cao.
- Cân nhắc bổ sung nhóm người bệnh có nguy cơ cao như bệnh nhi, phụ nữ mang thai và người cao tuổi.
- Cân nhắc bổ sung nhóm người bệnh có yếu tố ảnh hưởng đến chuyển hóa hoặc thải trừ của thuốc như người bệnh suy gan hoặc suy thận.
- Tăng cường giám sát người bệnh (ví dụ: theo dõi lâm sàng để đảm bảo phát hiện và xử lý kịp thời khi xuất hiện biến cố bất lợi trong quá trình điều trị).
- Triển khai hoạt động giám sát điều trị thông qua nồng độ thuốc trong máu với các thuốc có khuyến cáo, bao gồm xét nghiệm và hiệu chỉnh liều theo kết quả định lượng.
- Trong điều kiện cho phép, cân nhắc làm tròn liều dùng đến số nguyên hoặc đơn vị liều gần nhất.
- Triển khai các khóa đào tạo chuyên môn, kỹ năng và năng lực chuyên sâu về kê đơn và sử dụng thuốc có nguy cơ cao.
- Yêu cầu bảo quản thuốc cụ thể để giảm thiểu sai sót.
- Thông tin, tư vấn và giáo dục người bệnh hoặc người chăm sóc về nguy cơ liên quan đến thuốc.
- Nếu có thay đổi về danh mục và hướng dẫn quản lý thuốc có nguy cơ cao, cần thông báo, cập nhật tới các nhân viên y tế liên quan về những thay đổi này.
* Chú ý khi kê đơn và sử dụng thuốc có nguy cơ cao Cần lưu ý những điểm sau khi kê đơn và sử dụng thuốc có nguy cơ cao:
- Ghi lại cân nặng của tất cả người bệnh vào bệnh án.
- Xác định rõ đường dùng thuốc. Tránh kê đơn thuốc với nhiều đường dùng khác nhau trong một đơn thuốc (ví dụ: vừa dùng đường tiêm, vừa dùng đường uống).
- Liều dùng cần được thể hiện rõ ràng theo đơn vị liều lượng hoặc liều trên thể tích dung dịch (ví dụ: mg/ml).
- Cân nhắc hiệu chỉnh liều khi kê đơn cho các người bệnh thừa cân, béo phì hoặc nhẹ cân, và người bệnh có yếu tố lâm sàng (như suy thận hoặc suy gan) có thể ảnh hưởng đến chuyển hóa và thải trừ thuốc.
- Lưu ý tuân thủ hướng dẫn sử dụng của các thuốc có liều dùng phức tạp và khoảng điều trị hẹp do có thể làm tăng nguy cơ xảy ra độc tính (ví dụ: kháng sinh aminoglycosid).
- Nên có hệ thống kiểm tra chéo việc kê đơn, cấp phát và xác định lại thuốc trước khi sử dụng cho người bệnh.
* Chiến lược giảm thiểu ADR liên quan đến thuốc có nguy cơ cao - Chiến lược can thiệp đơn lẻ ít có khả năng dự phòng ADR liên quan đến thuốc có nguy cơ cao. Do đó, cần xem xét phối hợp nhiều chiến lược can thiệp để thúc đẩy việc sử dụng thuốc an toàn, giảm khả năng mắc lỗi hoặc sai sót trong quá trình sử dụng thuốc. Nên sử dụng các chiến lược có thể tác động được vào nhiều bước của chu trình quản lý và sử dụng thuốc bao gồm bảo quản, kê đơn, cấp phát, thực hiện thuốc và theo dõi đáp ứng của người bệnh. Kết hợp các chiến lược can thiệp mức độ thấp (như đào tạo/tập huấn, cung cấp thông tin thuốc cho nhân viên y tế) với các chiến lược can thiệp mức độ cao như quy định bắt buộc, quy định đảm bảo an toàn, chuẩn hóa quy trình, đơn giản hóa, giới hạn tiếp cập hoặc sử dụng thuốc tuỳ theo loại thuốc và điều kiện triển khai của cơ sở khám bệnh, chữa bệnh. - Một số biện pháp có thể cân nhắc để giảm thiểu nguy cơ liên quan đến thuốc có nguy cơ cao:
- Tính toán trước liều dùng của thuốc với dạng thuốc tương ứng trước khi sử dụng thuốc.
- Tính nồng độ thuốc trong dung dịch.
- Đảm bảo thiết bị truyền dịch được mặc định cài đặt chế độ an toàn nhất.
- Khi chuyển người bệnh sang khoa/phòng hay đơn vị điều trị khác, cần thông báo cho đơn vị tiếp nhận các thuốc có nguy cơ cao đang sử dụng trên người bệnh.
- Sử dụng các biện pháp nhắc nhở, bảng kiểm, dán cảnh báo. Nên tích hợp vào hệ thống công nghệ thông tin nếu điều kiện cho phép.
- Các yêu cầu về bảo quản hoặc thực hành cụ thể với thuốc (xem Phụ lục 12).
- Thường xuyên đánh giá các sự cố và các lỗi có thể bị bỏ qua trong hệ thống. Sử dụng phân tích tiến cứu và thiết kế lại hệ thống để dự phòng lặp lại các lỗi tương tự.
c) Quản lý người bệnh có nguy cơ cao
- Xác định và theo dõi sát người bệnh có nguy cơ cao xuất hiện ADR (xem Phụ lục 12). Các yếu tố nguy cơ thuộc người bệnh liên quan đến ADR bao gồm:
- Sử dụng đồng thời nhiều thuốc.
- Độ tuổi (ví dụ: trẻ sơ sinh, bệnh nhi và người cao tuổi).
- Tình trạng bệnh mắc kèm (ví dụ: suy thận, suy gan).
- Mức độ nghiêm trọng của bệnh.
- Tiền sử dị ứng hoặc gặp ADR trước đó.
- Thay đổi dược động học/dược lực học.
- Lưu ý người bệnh có tiền sử gặp ADR và/hoặc dị ứng thuốc, bác sĩ, người kê đơn thuốc hoặc nhân viên y tế khác có thẩm quyền cần lưu ý khai thác kỹ tiền sử dị ứng thuốc, dị nguyên của người bệnh trước khi kê đơn thuốc hoặc chỉ định sử dụng thuốc theo quy định tại Phụ lục VI ban hành kèm Thông tư số 51/2017/TT-BYT ngày 29 tháng 12 năm 2017 của Bộ trưởng Bộ Y tế về Hướng dẫn phòng, chẩn đoán và xử trí phản vệ. Tất cả thông tin liên quan đến dị ứng, dị nguyên phải được ghi vào sổ khám bệnh, bệnh án, giấy ra viện, giấy chuyển viện. - Khi đã xác định được thuốc gây ra phản ứng có hại trên người bệnh:
- Với các ADR là phản vệ, bác sĩ, nhân viên y tế phải cấp cho người bệnh thẻ theo dõi dị ứng ghi rõ tên thuốc hoặc dị nguyên gây dị ứng theo hướng dẫn tại Phụ lục VII ban hành kèm theo Thông tư số 51/2017/TT-BYT ngày 29 tháng 12 năm 2017 của Bộ trưởng Bộ Y tế, giải thích kỹ và nhắc người bệnh cung cấp thông tin này cho bác sĩ, nhân viên y tế mỗi khi khám bệnh, chữa bệnh.
- Với các ADR nghiêm trọng khác, nhân viên y tế cân nhắc có thể cấp “Thẻ cảnh báo phản ứng có hại của thuốc” cho người bệnh theo mẫu tại Phụ lục 2.2
– Hướng dẫn Quốc gia về Cảnh giác Dược ban hành kèm theo Quyết định số 122/QĐ-BYT ngày 11 tháng 01 năm 2021 của Bộ trường Bộ Y tế. Thẻ này giúp thông báo cho tất cả nhân viên y tế nhận biết người mang thẻ đã từng gặp phản ứng có hại của thuốc nghiêm trọng. Thẻ cũng giúp người bệnh biết về những phản ứng nghiêm trọng của họ. Người bệnh nên mang theo thẻ này và xuất trình cho nhân viên y tế trong tất cả những lần khám bệnh. Biện pháp này giúp nhân viên y tế biết được tiền sử bệnh liên quan đến thuốc của người bệnh và giúp tránh phản ứng có hại tương tự.
d) Thông tin thuốc cho nhân viên y tế và người bệnh
* Thông tin thuốc cho nhân viên y tế - Các nội dung thông tin thuốc cần cung cấp cho nhân viên y tế bao gồm chỉ định, chống chỉ định, cách dùng, tác dụng không mong muốn (tỷ lệ ghi nhận ADR trong y văn, yếu tố nguy cơ, biện pháp xử trí và dự phòng), tương tác thuốc và theo dõi khi sử dụng thuốc. - Thông tin về tiền sử sử dụng thuốc và thông tin lâm sàng của người bệnh cần được cung cấp đầy đủ khi chuyển người bệnh giữa các cơ sở điều trị khác nhau. - Thông tin thuốc đặc biệt cần thiết trong các trường hợp:
- Thuốc mới được cấp số đăng ký lưu hành hoặc thuốc có ít thông tin có thể tra cứu được.
- Thuốc có đi kèm những yêu cầu đặc biệt để giảm thiểu hậu quả bất lợi trên người bệnh.
- Thuốc mà nhân viên y tế còn ít kinh nghiệm trong quá trình sử dụng.
- Nguồn tra cứu thông tin về thuốc có thể tham khảo Chương 8. Thông tin thuốc trong hoạt động Cảnh giác Dược - Hướng dẫn Quốc gia về Cảnh giác Dược năm 2021. - Hình thức cung cấp thông tin: trao đổi trực tiếp với nhân viên y tế, công văn thông báo tới các khoa lâm sàng, trao đổi trong họp giao ban, cập nhật thông tin trên Bản tin Thông tin thuốc và tổ chức đào tạo, tập huấn cho nhân viên y tế.
* Thông tin thuốc cho người bệnh - Với người bệnh, việc cung cấp thông tin và tư vấn sử dụng thuốc nên được thực hiện với tất cả các thuốc mới bắt đầu sử dụng trong cơ sở khám bệnh, chữa bệnh, đặc biệt là các thuốc có nguy cơ cao và các thuốc tiếp tục được sử dụng sau khi xuất viện. Ghi chép và cập nhật lịch sử sử dụng thuốc của người bệnh giúp đảm bảo an toàn khi kê đơn và sử dụng thuốc. Tiền sử sử dụng thuốc tốt nhất là danh sách tất cả các loại thuốc mà người bệnh đã sử dụng trước khi nhập viện và khai thác được từ việc phỏng vấn người bệnh và/hoặc người chăm sóc (nếu có điều kiện khai thác). Ưu tiên cung cấp thông tin và tư vấn sử dụng thuốc cho người bệnh hoặc người chăm sóc trong các trường hợp sau:
- Người bệnh cao tuổi.
- Người bệnh được kê đơn đồng thời nhiều thuốc.
- Người bệnh được chỉ định nhiều liều thuốc trong ngày.
- Người bệnh được kê các thuốc có nguy cơ cao.
- Người bệnh phải thay đổi phác đồ điều trị.
- Người bệnh có suy giảm chức năng gan, thận.
- Người bệnh gặp trở ngại trong việc sử dụng thuốc như khó nuốt, khó cử động, nhìn mờ, lú lẫn hoặc có các bất thường khác về mặt nhận thức.
- Người bệnh có khả năng không tuân thủ điều trị.
- Thông tin cần cung cấp cho người bệnh liên quan đến ADR bao gồm:
- Các dấu hiệu/biểu hiện bất thường khi sử dụng thuốc.
- Thời gian xuất hiện ADR.
- Biện pháp xử trí với ADR ở mức độ nhẹ (người bệnh có thể tự xử trí). Trường hợp ADR ở mức độ nặng cần khuyến cáo người bệnh liên hệ bác sĩ điều trị để được tư vấn hoặc nhập viện để xử trí cấp cứu.
- Biện pháp dự phòng ADR. Ví dụ: trường hợp người bệnh đã được cấp thẻ dị ứng thì lưu ý không được sử dụng lại thuốc gây dị ứng.
- Hình thức cung cấp thông tin: tư vấn trực tiếp, có thể kèm theo tờ rời hướng dẫn sử dụng thuốc và theo dõi ADR.
đ) Đào tạo, tập huấn cho nhân viên y tế
- Nhân viên y tế cần cập nhật liên tục về kiến thức và kỹ năng thực hành Cảnh giác Dược, sử dụng thuốc hợp lý, an toàn thông qua các chương trình đào tạo, tập huấn phối hợp với điều kiện thực tế tại cơ sở khám bệnh, chữa bệnh. - Hình thức đào tạo, tập huấn cho nhân viên y tế có thể bao gồm:
- Lớp đào tạo liên tục do chuyên gia về dược lý, dược lâm sàng hoặc lâm sàng giảng dạy.
- Lớp đào tạo liên tục của các trường Đại học Y Dược tổ chức.
- Đào tạo dưới hình thức giao ban chuyên môn, sinh hoạt khoa học hoặc hội thảo khoa học tại cơ sở khám bệnh, chữa bệnh.
- Đào tạo trong quá trình đi buồng bệnh.
- Đào tạo bằng các bản tin cập nhật về thuốc tại cơ sở khám bệnh, chữa bệnh.
- Đào tạo qua trao đổi thông tin trực tiếp giữa các nhân viên y tế.
e) Đánh giá sử dụng thuốc
- Đánh giá sử dụng thuốc là hoạt động nên được thực hiện thường xuyên, có hệ thống, dựa trên các tiêu chí giúp cho đảm bảo sử dụng thuốc phù hợp (ở mức từng cá thể người bệnh). Mục đích của đánh giá sử dụng thuốc là thúc đẩy tối ưu hóa điều trị thông qua việc đảm bảo việc sử dụng thuốc là phù hợp với các chuẩn mực chăm sóc sức khỏe hiện hành. Nếu việc việc sử dụng thuốc không phù hợp, cần triển khai can thiệp phù hợp để điều chỉnh lại. Đánh giá sử dụng thuốc nghĩa là đánh giá quá trình thực tế trong kê đơn, cấp phát hoặc dùng thuốc (chỉ định, liều dùng, tương tác thuốc…) trên từng người bệnh cụ thể. - Các mục tiêu cụ thể của đánh giá sử dụng thuốc:
- Xây dựng các hướng dẫn (tiêu chí) cho sử dụng thuốc hợp lý.
- Đánh giá hiệu quả của điều trị bằng thuốc.
- Nâng cao tính trách nhiệm trong quá trình sử dụng thuốc.
- Ngăn chặn các vấn đề liên quan đến sử dụng thuốc, trong đó bao gồm phản ứng có hại của thuốc, quá liều, không đủ liều, liều không đúng, thất bại điều trị và dùng thuốc không có trong danh mục.
- Phát hiện ra những lĩnh vực cần tăng cường cung cấp thông tin và các biện pháp truyền thông.
Trong lĩnh vực đảm bảo an toàn thuốc, các nghiên cứu về đánh giá sử dụng thuốc có thể tập trung vào các khía cạnh như đánh giá và/hoặc giám sát hành vi kê đơn một thuốc cụ thể (chỉ định, liều, cách dùng), báo cáo sai sót trong điều trị, báo cáo về phản ứng có hại của thuốc, thuốc có phạm vi điều trị hẹp, thuốc có tần suất gặp phản ứng có hại cao, thuốc sử dụng theo chỉ định chưa được cấp phép (off label), thuốc sử dụng cho nhóm người bệnh có nguy cơ cao. Việc đánh giá sử dụng thuốc nếu được triển khai định kỳ sẽ giúp phát hiện nguy cơ hay sai sót liên quan đến thuốc có thể phòng tránh được. g) Cập nhật, sửa đổi hướng dẫn sử dụng thuốc
Tùy thuộc vào vấn đề liên quan đến sử dụng thuốc được đánh giá có phải là ADR hay tác dụng phụ của thuốc (bao gồm cả sai sót trong quá trình sử dụng thuốc) hay khiếm khuyết chất lượng thuốc, dược sĩ lâm sàng tư vấn cho Hội đồng Thuốc và điều trị hoặc người chịu trách nhiệm chuyên môn kỹ thuật của cơ sở khám bệnh, chữa bệnh sửa đổi, cập nhật hướng dẫn sử dụng thuốc trong cơ sở khám bệnh, chữa bệnh như giới hạn chỉ định, hướng dẫn sử dụng một số thuốc có nguy cơ cao (như thuốc cản quang, thuốc gây mê, …), tạm ngừng sử dụng hoặc ngừng sử dụng vĩnh viễn với các trường hợp xảy ra chuỗi ADR liên quan đến cùng một lô thuốc hoặc khi ghi nhận các vấn đề liên quan đến chất lượng thuốc. Đây là giải pháp can thiệp hiệu quả để giảm thiểu nguy cơ xảy ra các vấn đề liên quan đến thuốc. Hướng dẫn sử dụng thuốc sau khi được cập nhật, sửa đổi cũng cần được thông báo tới nhân viên y tế để triển khai thực hiện. 3.6.2. Đánh giá tác động của kế hoạch giảm thiểu ADR
- Trong một số trường hợp, việc triển khai kế hoạch giảm thiểu ADR cần đi kèm với đánh giá hiệu quả của hoạt động này. Việc triển khai các can thiệp giảm thiểu ADR có vai trò quan trọng để đảm bảo sử dụng thuốc hợp lý, an toàn. Hiệu quả tác động của can thiệp có thể xác định thông qua các chỉ số quá trình (trước và sau khi can thiệp), lợi ích lâm sàng và lợi ích kinh tế. Tác động và hiệu quả của một hay nhiều can thiệp liên quan an toàn thuốc nên được đánh giá từ góc độ hiệu quả trên người bệnh. Thành công của chương trình an toàn thuốc có thể xác định được bằng quy trình đo lường, mục tiêu đầu ra hoặc chỉ tiêu can thiệp đã xác định. - Việc lựa chọn được can thiệp phù hợp đóng vai trò quan trọng. Các can thiệp liệt kê ở mục 3.6.1 của Hướng dẫn này có thể được coi là tiêu chuẩn đánh giá tạm thời và cần kết nối với kết quả lâm sàng. Hoạt động can thiệp có thể liên quan đến kết quả lâm sàng (ví dụ: số tai biến liên quan đến thuốc đã xảy ra) hoặc khối lượng công việc (ví dụ: số lượng hướng dẫn đã được rà soát, đánh giá). Tiêu chuẩn đánh giá kết cục khó thu thập thông tin hơn và thường cần phải hiệu chỉnh theo các yếu tố nguy cơ (ví dụ: tỷ lệ tử vong, tỷ lệ tái nhập viện). - Đánh giá hiệu quả can thiệp là bước cuối cùng trong quy trình quản lý an toàn thuốc. Một số phương pháp thường được áp dụng để đánh giá hiệu quả của can thiệp bao gồm: - Kiểm tra hiệu quả chương trình truyền thông: Kiểm tra xem người bệnh và nhân viên y tế có nhận được thông tin và hiểu được toàn bộ thông tin hay không.
- Phân tích tác động lên việc kê đơn của thầy thuốc: Phân tích xem việc kê đơn thay đổi như thế nào sau khi có can thiệp.
- Theo dõi các báo cáo tự nguyện: Các báo cáo về biến cố bất lợi có còn tiếp tục xảy ra sau khi tiến hành can thiệp hay không.
- Thực hiện các nghiên cứu mô tả về tình hình kê đơn và các biến cố bất lợi: Các can thiệp có làm giảm tỷ lệ mắc/ tỷ lệ tử vong do ADR gây ra hay không.
- Nếu các can thiệp giảm thiểu ADR không cho thấy hiệu quả đối với các ADR quan trọng, cơ sở khám bệnh, chữa bệnh nên có biện pháp bổ sung/thay thế các can thiệp khác phù hợp nếu thuốc tiếp tục được sử dụng tại đơn vị. - Một số chỉ số áp dụng trong đánh giá hiệu quả của hoạt động giám sát ADR tại cơ sở khám bệnh, chữa bệnh (xem Phụ lục 13). IV. TỔ CHỨC THỰC HIỆN
Triển khai hoạt động giám sát ADR trong cơ sở khám bệnh, chữa bệnh cần có sự tham gia của nhiều đối tác đa ngành bao gồm người đứng đầu cơ sở khám bệnh, chữa bệnh, Hội đồng Thuốc và điều trị (nếu có), các phòng chức năng, các khoa lâm sàng (hoặc khoa, phòng khám bệnh), khoa, phòng cận lâm sàng và khoa Dược (hoặc bộ phận Dược lâm sàng). Giám sát phản ứng có hại của thuốc là trách nhiệm của tất cả các nhân viên y tế bao gồm bác sĩ, dược sĩ, điều dưỡng viên, hộ sinh viên, kỹ thuật viên và các nhân viên y tế khác có liên quan đến sử dụng thuốc tại cơ sở khám bệnh, chữa bệnh. 4.1. Người đứng đầu cơ sở khám bệnh, chữa bệnh
- Tổ chức và triển khai hoạt động giám sát ADR trong đơn vị. - Giám sát việc lập kế hoạch, triển khai và đánh giá các kế hoạch giám sát và giảm thiểu ADR. - Chỉ đạo xây dựng và triển khai các hoạt động dự phòng phản ứng có hại của thuốc và các vấn đề liên quan đến thuốc dựa trên các hướng dẫn thực hành, khuyến cáo từ y văn, báo cáo về sai sót, các công cụ giám sát an toàn thuốc và phân tích dữ liệu an toàn thuốc của đơn vị. - Chỉ đạo việc đảm bảo việc quản lý, sử dụng thuốc và an toàn cho người bệnh là cốt lõi của chiến lược đảm bảo chất lượng điều trị của đơn vị. - Chỉ đạo việc xây dựng “văn hóa an toàn” thông qua đào tạo, tập huấn và truyền thông các “bài học kinh nghiệm” trong đơn vị. - Chỉ đạo việc đảm bảo tuân thủ các quy định của pháp luật và quy chế chuyên môn về an toàn thuốc. 4.2. Tiểu ban giám sát ADR - Hội đồng Thuốc và điều trị/Bộ phận Dược lâm sàng tại cơ sở khám bệnh, chữa bệnh không tổ chức khoa Dược.
- Xây dựng quy trình phát hiện, đánh giá, xử trí, dự phòng ADR và các sai sót trong chu trình cung ứng, sử dụng thuốc tại cơ sở khám bệnh, chữa bệnh từ giai đoạn xây dựng danh mục thuốc đến kê đơn của bác sĩ, chuẩn bị và cấp phát thuốc của dược sĩ, thực hiện y lệnh và hướng dẫn sử dụng của điều dưỡng, sự tuân thủ điều trị của người bệnh nhằm bảo đảm an toàn cho người bệnh trong quá trình điều trị. - Tổ chức giám sát ADR, ghi nhận và rút kinh nghiệm các sai sót trong điều trị: - Xây dựng quy trình sử dụng thuốc, tổ chức giám sát chặt chẽ việc sử dụng các thuốc có nguy cơ cao xuất hiện ADR và việc sử dụng thuốc trên các đối tượng người bệnh có nguy cơ cao xảy ra ADR;
- Tổ chức hội chẩn, thảo luận và đánh giá để có kết luận xử trí và các biện pháp dự phòng trong trường hợp xảy ra các phản ứng có hại nghiêm trọng, các sai sót trong điều trị tại cơ sở khám bệnh, chữa bệnh;
- Đánh giá định kỳ, trình lãnh đạo cơ sở khám bệnh, chữa bệnh phê duyệt và và chia sẻ thông tin cho các bên liên quan báo cáo tổng kết về ADR và các sai sót trong điều trị ghi nhận tại đơn vị mình.
- Triển khai hệ thống báo cáo ADR trong cơ sở khám bệnh, chữa bệnh: - Đối với ADR gây tử vong, đe dọa tính mạng, ADR xảy ra liên tiếp với một sản phẩm thuốc hay ADR với các thuốc mới đưa vào sử dụng trong cơ sở khám bệnh, chữa bệnh: nhân viên y tế báo cáo ADR với khoa Dược hoặc bộ phận Dược lâm sàng tập hợp để có cơ sở trình người chịu trách nhiệm chuyên môn kỹ thuật của cơ sở khám bệnh, chữa bệnh có quyết định xử lý kịp thời, phù hợp và trong thời gian sớm nhất gửi báo cáo về Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
- Đối với ADR khác: khuyến khích nhân viên y tế báo cáo, khoa Dược hoặc bộ phận Dược lâm sàng tổng hợp và gửi báo cáo lên Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
- Thông tin cho nhân viên y tế trong cơ sở khám bệnh, chữa bệnh về ADR, sai sót trong sử dụng thuốc để kịp thời rút kinh nghiệm chuyên môn. - Xác định danh mục thuốc có nguy cơ cao cần giám sát để đảm bảo an toàn trong quá trình sử dụng thuốc và xây dựng quy trình theo dõi, hướng dẫn sử dụng các thuốc này tại cơ sở khám bệnh, chữa bệnh. - Cập nhật, bổ sung, sửa đổi danh mục thuốc của cơ sở khám bệnh, chữa bệnh, hướng dẫn điều trị và các quy trình chuyên môn khác dựa trên thông tin về ADR và sai sót trong sử dụng thuốc ghi nhận được tại cơ sở khám bệnh, chữa bệnh và từ các cảnh báo của các cơ quan quản lý và chuyên môn của Bộ Y tế. - Tổ chức tập huấn định kỳ cho nhân viên y tế của cơ sở khám bệnh, chữa bệnh về kỹ năng phát hiện, xử trí ADR, kỹ năng điền báo cáo ADR đúng và đầy đủ thông tin. 4.3. Khoa Dược
- Cập nhật thông tin sử dụng thuốc, thông tin về thuốc mới, thông tin về an toàn thuốc gửi đến nhân viên y tế và người bệnh trong cơ sở khám bệnh, chữa bệnh dưới nhiều hình thức như tư vấn chuyên môn trực tiếp, sinh hoạt khoa học, cung cấp bản tin, thông tin về thuốc và các tài liệu chuyên môn thông tin thuốc khác. - Giám sát chất lượng thuốc trong quá trình sử dụng thuốc tại bệnh viện. - Tham gia xây dựng và sửa đổi quy trình giám sát và báo cáo ADR tại đơn vị. - Xác định các thuốc có nguy cơ cao và người bệnh có nguy cơ cao xuất hiện ADR tại đơn vị. - Trong quá trình thực hiện hoạt động chuyên môn, thông qua xem bệnh án hoặc duyệt thuốc tại Khoa Dược, phát hiện ADR dựa trên các thuốc có khả năng được sử dụng để xử trí phản ứng có hại của thuốc, biểu hiện lâm sàng và kết quả xét nghiệm cận lâm sàng bất thường (xem Phụ lục 2). Ưu tiên xem xét bệnh án của người bệnh có nguy cơ cao và người bệnh sử dụng thuốc có nguy cơ cao xảy ra ADR (xem Phụ lục 11 và Phụ lục 12). - Trao đổi với bác sĩ, điều dưỡng nếu phát hiện ADR khi thực hiện hoạt động Dược lâm sàng tại khoa phòng để có biện pháp xử trí phù hợp. - Cung cấp thông tin về thuốc trong quá trình xác định và xử trí ADR theo yêu cầu của nhân viên y tế. - Phân tích/đánh giá các báo cáo ADR và tổng kết định kỳ dữ liệu báo cáo ADR tại đơn vị. - Phổ biến các thông tin thu được thông qua chương trình giám sát ADR cho nhân viên y tế và người bệnh, đặc biệt các ADR nghiêm trọng và ADR không định trước. - Hướng dẫn, hỗ trợ bác sĩ và điều dưỡng viên hoàn thiện đầy đủ và chính xác các thông tin cần thiết trong mẫu báo cáo phản ứng có hại của thuốc. - Dược sĩ có thể trực tiếp thu thập thông tin và viết báo cáo ADR. - Lưu thư cảm ơn đã nhận được báo cáo và thư phản hồi kết quả thẩm định báo cáo ADR của Trung tâm Quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc gửi cho nhân viên y tế đã tham gia báo cáo. 4.4. Phòng Quản lý chất lượng
- Xây dựng kế hoạch và nội dung hoạt động quản lý chất lượng trong cơ sở khám bệnh, chữa bệnh. - Phối hợp với Phòng Kế hoạch tổng hợp và các đơn vị có liên quan để thực hiện, theo dõi, kiểm tra, đánh giá các hoạt động liên quan đến cải tiến chất lượng và an toàn người bệnh. - Phối hợp với các đơn vị kiểm tra, đánh giá việc tuân thủ quy định, quy chế chuyên môn. - Tổ chức đánh giá chất lượng cơ sở khám bệnh, chữa bệnh dựa trên các bộ tiêu chí do Bộ Y tế ban hành, bao gồm các tiêu chí liên quan đến an toàn thuốc. 4.5. Phòng Kế hoạch tổng hợp
- Phối hợp với các khoa/phòng tổ chức, theo dõi, đánh giá hiệu quả việc thực hiện kế hoạch đảm bảo an toàn trong sử dụng thuốc tại bệnh viện. - Tổng kết đánh giá công tác chuyên môn, triển khai nghiên cứu khoa học liên quan an toàn thuốc. - Phối hợp tổ chức đào tạo liên tục cho nhân viên y tế về hoạt động giám sát phản ứng có hại của thuốc và các vấn đề liên quan đến thuốc. 4.6. Khoa lâm sàng, khoa, phòng khám bệnh và khoa cận lâm sàng
- Phát hiện và xử trí ADR. - Khoa lâm sàng, khoa, khòng khám bệnh: tuân thủ các hướng dẫn về đảm bảo an toàn trong sử dụng thuốc theo quy định. - Khoa cận lâm sàng: phối hợp với khoa lâm sàng và khoa Dược để giám sát các phản ứng có hại của thuốc và các vấn đề liên quan đến thuốc thông qua kết quả xét nghiệm cận lâm sàng hoặc kết quả chẩn đoán hình ảnh. 4.7. Nhân viên y tế
Tùy theo chức năng, nhiệm vụ cụ thể, các nhân viên y tế liên quan có trách nhiệm triển khai thực hiện: - Tuân thủ chỉ định, chống chỉ định, thận trọng, liều dùng của thuốc, chú ý tiền sử dị ứng (bao gồm tiền sử dị ứng thuốc) của người bệnh, tương tác thuốc trong kê đơn và thực hiện đầy đủ việc giám sát theo dõi người bệnh trong quá trình điều trị để đảm bảo kê đơn thuốc hợp lý (xem Phụ lục 10).
- Tuân thủ cảnh báo và thận trọng khi kê đơn sử dụng các thuốc có nguy cơ cao hoặc kê đơn trên đối tượng người bệnh có nguy cơ cao (xem Phụ lục 11).
- Tuân thủ quy trình bảo quản và sử dụng thuốc cho người bệnh.
- Kiểm tra tương tác thuốc, chống chỉ định, trùng lặp hoạt chất/nhóm dược lý trong quy trình cấp phát và sử dụng thuốc.
- Báo cáo ADR theo quy định khi phát hiện, ghi nhận phản ứng xảy ra trên người bệnh.
- Đánh giá mức độ nghiêm trọng của ADR để quyết định hướng xử trí lâm sàng phù hợp.
- Phân tích nguyên nhân để xác định thuốc nghi ngờ. Giảm liều hoặc ngừng thuốc nghi ngờ gây ADR trong điều kiện lâm sàng cho phép.
- Kịp thời thực hiện các biện pháp điều trị triệu chứng, điều trị hỗ trợ, đảm bảo chức năng sống còn cho người bệnh.
- Thực hiện theo các hướng dẫn chuyên môn của Bộ Y tế có liên quan nếu việc xử trí ADR thuộc phạm vi các hướng dẫn đó (ví dụ: Thông tư số 51/2017/TTBYT ngày 29 tháng 12 năm 2017 của Bộ trưởng Bộ Y tế về Hướng dẫn phòng, chẩn đoán và xử trí phản vệ).
- Trong trường hợp cần thiết, trao đổi hướng xử trí với đồng nghiệp, tổ chức hội chẩn chuyên môn, tham khảo thêm thông tin về ADR từ bộ phận Dược lâm sàng hoặc các Trung tâm về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc.
- Giám sát chặt chẽ người bệnh trong trường hợp bắt buộc sử dụng lại thuốc nghi ngờ gây ADR khi không có thuốc thay thế hoặc khi lợi ích của thuốc vượt trội hơn nguy cơ.
- Đảm bảo thông tin của phản ứng có hại nghi ngờ do thuốc được ghi chép vào hồ sơ bệnh án, bao gồm cả hệ thống cấp phát và kê đơn điện tử (nếu có).
CÁC PHỤ LỤC
PHỤ LỤC 1. PHÂN LOẠI KHUYẾN CÁO THỰC HIỆN HOẠT ĐỘNG GIÁM SÁT ADR
| Các hoạt động chính | Mức độ khuyến cáo thực hiện | Nội dung tham khảo | Trang |
| Cần phải thực hiện | Khuyến khích thực hiện |
| 1. Phân công bộ phận/người phụ trách giám sát ADR | x | | 3.1 | 8 |
| 2. Xây dựng quy trình giám sát ADR | x | | 3.2 | 9 |
| 3. Phát hiện ADR | | | | |
| 3.1. Phát hiện ADR thông qua hoạt động thường quy | x | | 3.3.1 | 10 |
| 3.2. Phát hiện ADR thông qua giám sát chủ động | | x | 3.3.2 | 10 |
| 4. Báo cáo ADR | | | | |
| Triển khai hệ thống báo cáo tự nguyện từ tất cả nhân viên y tế trong cơ sở khám bệnh, chữa bệnh | x | | 3.4 | 13 |
| 5. Đánh giá ADR | | | | |
| 5.1. Đánh giá mức độ nghiêm trọng | x | | 3.5.1 | 19 |
| 5.2. Đánh giá mức độ nặng | | x | 3.5.2 | 19 |
| 5.3. Đánh giá mối quan hệ nhân quả | | x | 3.5.3 | 20 |
| 5.4. Đánh giá khả năng phòng tránh được | | x | 3.5.4 | 20 |
| 5.5. Tổng kết dữ liệu ADR định kỳ | x x x | x x | 3.5.5 | 22 |
| - Số lượng báo cáo - Đặc điểm thuốc nghi ngờ - Đặc điểm ADR |
| - Đánh giá chất lượng báo cáo - Phân tích xu hướng ADR, xu hướng tỷ lệ ADR |
| 6. Dự phòng ADR | | | | |
| 6.1. Xây dựng và triển khai kế hoạch giảm thiểu ADR | | | | |
| 6.1.1. Xây dựng được hệ thống các danh mục thuốc cần lưu ý - Danh mục nhìn giống nhau, đọc giống nhau - Danh mục thuốc không nhai, nghiền, bẻ - Danh mục tương tác thuốc - Danh mục tương hợp, tương kỵ - Danh mục thuốc cần hiệu chỉnh liều - Danh mục cách pha, bảo quản và sử dụng các thuốc tiêm truyền | x | x x x x x | 3.6.1 | 23 |
| 6.1.2. Quản lý thuốc có nguy cơ cao | x | x |
| - Xây dựng danh mục thuốc có nguy cơ cao |
| - Xây dựng hướng dẫn quản lý thuốc có nguy cơ cao |
| 6.1.3. Quản lý người bệnh có nguy cơ cao | | x |
| 6.1.4. Đào tạo, tập huấn cho nhân viên y tế về Cảnh giác Dược và giám sát ADR | x | |
| 6.1.5. Thông tin thuốc cho nhân viên y tế và cho người bệnh (trong đó có thông tin về ADR) | x | |
| 6.1.6. Đánh giá sử dụng thuốc | | x |
| 6.1.7. Cập nhật, sửa đổi hướng dẫn sử dụng thuốc | | x |
| 6.2. Đánh giá tác động của kế hoạch giảm thiểu ADR | | x | 3.6.2 | 29 |
PHỤ LỤC 2. MỘT SỐ BIỂU HIỆN LÂM SÀNG VÀ CẬN LÂM SÀNG BẤT THƯỜNG CÓ THỂ LIÊN QUAN ĐẾN PHẢN ỨNG CÓ HẠI CỦA THUỐC
1. Một số biểu hiện chung
- Sốt. - Đau đầu. - Buồn ngủ. - Ngất. - Tăng cân nhanh.
2. Phản ứng ngoài da
- Mày đay. - Phù mạch. - Ban đỏ. - Ban xuất huyết. - Tăng nhạy cảm ánh sáng. - Ban nổi bọng: Hồng ban đa dạng, hội chứng Stevens-Johnson, hoại tử biểu bì nhiễm độc, ban cố định. - Mụn trứng cá. - Rụng tóc. - Nhiễm khuẩn, nhiễm nấm.
3. Rối loạn chức năng gan
- Vàng da, vàng mắt, phù. - Kết quả xét nghiệm chức năng gan bất thường (tăng AST, ALT, phosphatase kiềm, bilirubin máu). - Suy gan.
4. Kết quả xét nghiệm huyết học bất thường.
- Giảm hồng cầu, hemoglobin. - Giảm bạch cầu, giảm bạch cầu đa nhân trung tính. - Giảm tiểu cầu. - Tăng bạch cầu ưa acid. - Thiếu máu tan máu. - Tăng số lượng bạch cầu lympho. - Phản ứng Coombs dương tính. - Giảm thời gian prothrombin, tăng INR. - Xuất huyết.
5. Biểu hiện phản vệ.
6. Suy thận cấp
- Tăng creatinin máu, giảm mức lọc cầu thận
7. Rối loạn tiêu hóa.
- Nôn, buồn nôn. - Khó nuốt. - Rối loạn vị giác. - Tăng sản lợi. - Khô miệng. - Loét miệng. - Loét thực quản. - Đau thượng vị. - Sỏi mật. - Viêm tụy. - Táo bón. - Tiêu chảy và viêm đại tràng giả mạc. - Xuất huyết tiêu hóa.
8. Rối loạn hô hấp
- Khó thở. - Co thắt phế quản. - Viêm phổi kẽ.
9. Giá trị glucose máu bất thường
- Tăng glucose máu. - Hạ glucose máu.
10. Rối loạn nội tiết
- Suy giáp. - Cường giáp. - Tăng prolactin máu. - Lupus ban đỏ do thuốc.
11. Rối loạn thần kinh, cơ
- Bệnh lý thần kinh ngoại biên. - Chóng mặt. - Co giật. - Rối loạn trương lực cơ. - Rối loạn ngoại tháp. - Tăng áp lực nội sọ. - Động tác bất thường. - Đau cơ. - Tiêu cơ vân cấp. - Loãng xương. - Hoại tử xương.
12. Huyết áp bất thường
- Hạ huyết áp. - Hạ huyết áp tư thế đứng. - Tăng huyết áp.
13. Rối loạn tim
- Loạn nhịp hoặc biểu hiện bất thường trên điện tâm đồ. - Viêm màng ngoài tim. - Chậm nhịp. - Huyết khối/ đột quỵ. - Bệnh cơ tim. - Bệnh van tim. - Suy tim.
14. Rối loạn tâm thần
- Trạng thái lú lẫn do thuốc. - Kích động. - Ức chế tâm thần. - Thay đổi tâm tính: trầm cảm, hưng cảm. - Rối loạn giấc ngủ. - Rối loạn hành vi ăn uống. - Rối loạn trí nhớ. - Thay đổi nhận thức. - Loạn thần. - Hội chứng cai thuốc.
15. Tất cả các biểu hiện bất thường khác ghi nhận được trong quá trình điều trị của người bệnh sau khi sử dụng thuốc nghi ngờ.
PHỤ LỤC 3. MẪU BÁO CÁO PHẢN ỨNG CÓ HẠI CỦA THUỐC
| (Ban hành kèm theo Thông tư số 23/2011/TT-BYT ngày 10/6/2011) |
| | BÁO CÁO PHẢN ỨNG CÓ HẠI CỦA THUỐC THÔNG TIN VỀ NGƯỜI BÁO CÁO, BỆNH NHÂN VÀ ĐƠN VỊ BÁO CÁO SẼ ĐƯỢC BẢO MẬT | Nơi báo cáo:…………………………………………… |
| Mã số báo cáo của đơn vị:…………………………… |
| | | Mã số báo cáo (do Trung tâm quốc gia quản lý): ………………………………………………………….. |
Xin anh/chị hãy báo cáo kể cả khi không chắc chắn về sản phẩm đã gây ra phản ứng và/hoặc không có đầy đủ các thông tin | A. THÔNG TIN VỀ BỆNH NHÂN | |
| 1. Họ và tên:………………………………........................... | 2. Ngày sinh:….../….../………… Hoặc tuổi:…………………........ | 3. Giới tính ¨ Nam ¨ Nữ | 4. Cân nặng: ……...….kg |
| B. THÔNG TIN VỀ PHẢN ỨNG CÓ HẠI (ADR) | |
| 5. Ngày xuất hiện phản ứng:……..../…….../……………… | 6. Phản ứng xuất hiện sau bao lâu (tính từ lần dùng cuối cùng của thuốc nghi ngờ):…………………………………………………………………………… |
| 7. Mô tả biểu hiện ADR | 8. Các xét nghiệm liên quan đến phản ứng |
| 9. Tiền sử (dị ứng, thai nghén, nghiện thuốc lá, nghiện rượu, bệnh gan, bệnh thận…) |
| 10. Cách xử trí phản ứng |
| 11. Mức độ nghiêm trọng của phản ứng |
| o Tử vong o Đe dọa tính mạng | | | o Nhập viện/Kéo dài thời gian nằm viện o Tàn tật vĩnh viễn/nặng nề | | o Dị tật thai nhi o Không nghiêm trọng | | | |
| 12. Kết quả sau khi xử trí phản ứng |
| o Tử vong do ADR o Tử vong không liên quan đến thuốc | | o Chưa hồi phục o Đang hồi phục | | o Hồi phục có di chứng o Hồi phục không có di chứng | | | o Không rõ |
| C. THÔNG TIN VỀ THUỐC NGHI NGỜ GÂY ADR | |
| STT | 13.Thuốc (tên gốc và tên thương mại) | Dạng BC, hàm lượng | Nhà sản xuất | Số lô | Liều dùng một lần | Số lần dùng trong ngày/ tuần/ tháng. | Đường dùng | Ngày điều trị (Ngày/tháng/năm) | Lý do dùng thuốc |
| Bắt đầu | Kết thúc |
| i | | | | | | | | | | |
| ii | | | | | | | | | | |
| iii | | | | | | | | | | |
| iv | | | | | | | | | | |
| STT (Tương ứng 13.) | 14.Sau khi ngừng/giảm liều của thuốc bị nghi ngờ, phản ứng có được cải thiện không? | 15.Tái sử dụng thuốc bị nghi ngờ có xuất hiện lại phản ứng không? |
| Có | | Không | Không ngừng/giảm liều | Không có thông tin | Có | Không | | Không tái sử dụng | Không có thông tin |
| i | o | | o | | o | | | o | | | o | o | | | | o | | o |
| ii | o | | o | | o | | | o | | | o | o | | | | o | | o |
| iii | o | | o | | o | | | o | | | o | o | | | | o | | o |
| iv | o | | o | | o | | | o | | | o | o | | | | o | | o |
| 16. Các thuốc dùng đồng thời (Ngoại trừ các thuốc dùng điều trị/khắc phục hậu quả của ADR) |
| Tên thuốc | Dạng bào chế, hàm lượng | Ngày điều trị (ngày/tháng/năm) | Tên thuốc | Dạng BC, hàm lượng | Ngày điều trị (ngày/tháng/năm) |
| Bắt đầu | Kết thúc | Bắt đầu | Kết thúc |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | |
| | | | | | | | | | | | | | | | | | | | | |
| D.PHẦN THẨM ĐỊNH ADR CỦA ĐƠN VỊ | |
| 17. Đánh giá mối liên quan giữa thuốc và ADR | | | | |
| o Chắc chắn o Có khả năng o Có thể | o Không chắc chắn o Chưa phân loại o Không thể phân loại | o Khác: …………………………..……… …………………………………………… …………………………………………… |
| 18. Đơn vị thẩm định ADR theo thang nào? | | | | |
| o Thang WHO | o Thang Naranjo | o Thang khác: ……………………………… |
| 19. Phần bình luận của nhân viên y tế (nếu có) |
| E. THÔNG TIN VỀ NGƯỜI BÁO CÁO | |
| 20. Họ và tên:………………………………….......................................... Nghề nghiệp/Chức vụ:……………………………………………… Điện thoại liên lạc:……………………………………………………… Email:…………………………………………………………………. |
| 21. Chữ ký | 22. Dạng báo cáo: o Lần đầu/ o Bổ sung | 23. Ngày báo cáo:………/…..…/………… |
Xin chân thành cảm ơn! Xin hãy báo cáo tất cả các phản ứng có hại mà anh/chị nghi ngờ, đặc biệt khi: - Các phản ứng liên quan tới thuốc mới
- Các phản ứng không mong muốn hoặc chưa được biết đến
- Các phản ứng nghiêm trọng
- Tương tác thuốc
- Thất bại trong điều trị
- Các vấn đề về chất lượng thuốc
- Các sai sót trong quá trình sử dụng thuốc.
Mẫu báo cáo này được áp dụng cho các phản ứng gây ra bởi: - Thuốc và các chế phẩm sinh học
- Vắc xin
- Các thuốc cổ truyền hoặc thuốc có nguồn gốc dược liệu
- Thực phẩm chức năng.
Người báo cáo có thể là: - Bác sĩ
- Dược sĩ
- Nha sĩ
- Y tá/điều dưỡng/nữ hộ sinh
- Các nhà cung cấp dịch vụ chăm sóc sức khỏe khác.
HƯỚNG DẪN LÀM BÁO CÁO Cách báo cáo: - Điền thông tin vào mẫu báo cáo
- Chỉ cần điền những phần anh/chị có thông tin
- Có thể đính kèm thêm một vài trang (nếu mẫu báo cáo không đủ khoảng trống để điền hay có những xét nghiệm liên quan).
- Xin hãy gửi báo cáo về Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng thuốc theo các địa chỉ sau:
| | Thư: Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hạ Trường Đại học Dược Hà Nội 13-15 Lê Thánh Tông, Quận Hoàn Kiếm, Hà Nội |
| | Fax: (024) 3933 5642 |
| | Điện thoại: (024) 3933 5618 |
| | Website: http://canhgiacduoc.org.vn Email: di.pvcenter@gmail.com |
Anh/chị có thể lấy mẫu báo cáo này tại khoa Dược, phòng Kế hoạch tổng hợp của bệnh viện hoặc tải từ trang web http://canhgiacduoc.org.vn. Nếu có bất kỳ thắc mắc nào, anh/chị có thể liên hệ với Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc theo số điện thoại (024) 3933 5618 hoặc theo địa chỉ email di.pvcenter@gmail.com.
| Phần dành cho Trung tâm DI & ADR Quốc gia |
| 1. Gửi xác nhận tới đơn vị báo cáo | o | 3. Phản ứng đã có trong y văn/SPC/CSDL | o |
| 2. Phân loại phản ứng o Thuốc mới o Thuốc cũ o Nghiêm trọng o Không nghiêm trọng | o | 4. Nhập dữ liệu vào hệ cơ sở dữ liệu quốc gia | o |
| 5. Nhập dữ liệu vào phần mềm Vigiflow | o |
| 6. Mức độ nghiêm trọng của phản ứng |
| o Đe dọa tính mạng/ gây tử vong | o Nhập viện/kéo dài thời gian nằm viện | o Gây dị tật/tàn tật | o Liên quan tới lạm dụng/phụ thuộc thuốc |
| 7. Gửi báo cáo tới hội đồng thẩm định | o | Ngày gửi .….../.…../………. | 8. Gửi báo cáo cho UMC | o | Ngày gửi ...…../….../……... |
| 9. Kết quả thẩm định | | | | | | | | | | | | | |
| o Chắc chắn o Có khả năng o Có thể | o Không chắc chắn o Chưa phân loại o Không thể phân loại | | | o Khác:…………………………………………………… ………………………………………………………...... ………………………………………………………….. |
| 10. Người quản lý báo cáo ………………………………………………………………… | 11. Ngày:….…./…..…/……….. | 12. Chữ ký |
| | | | | | | | | | | | | | |
PHỤ LỤC 4. VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH
Có thể tham khảo mẫu báo cáo phản ứng dị ứng thuốc dưới đây để xây dựng mẫu báo cáo ADR có chủ đích liên quan đến vấn đề an toàn thuốc cần triển khai giám sát tích cực tại cơ sở khám bệnh, chữa bệnh. [caption id="attachment_54241" align="alignnone" widthx="950"]
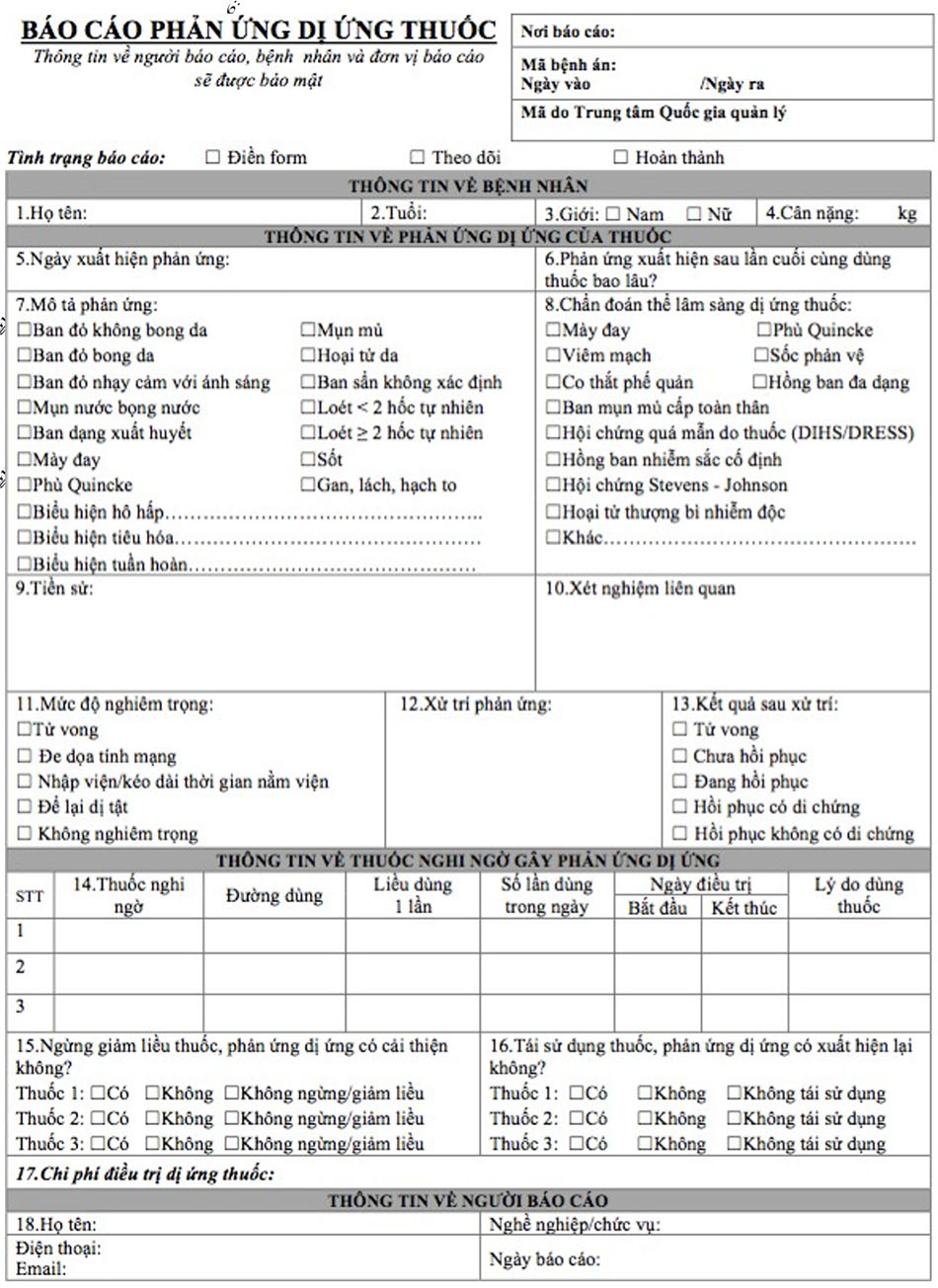
VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH[/caption]
PHỤ LỤC 5. DANH SÁCH MỘT SỐ THUỐC, XÉT NGHIỆM VÀ BIỂU HIỆN LÂM SÀNG LÀ DẤU HIỆU PHÁT HIỆN ADR
| Dấu hiệu phát hiện | Gợi ý nguyên nhân |
| Thuốc |
| Kháng histamin | Dị ứng thuốc |
| Adrenalin | Phản vệ hoặc xuất huyết do thuốc |
| Vitamin K | Quá liều thuốc chống đông kháng vitamin K |
| Protamin | Quá liều thuốc chống đông heparin/heparin trọng lượng phân tử thấp |
| Flumazenil | Quá liều thuốc an thần nhóm benzodiazepin |
| Fab miễn dịch với digoxin | Ngộ độc digoxin |
| Thuốc chống nôn | Buồn nôn/nôn liên quan đến sử dụng thuốc |
| Naloxon | Quá liều thuốc giảm đau opioid |
| Thuốc điều trị tiêu chảy | Tiêu chảy do nguyên nhân kháng sinh. Tìm kháng nguyên Clostridium difficile trong phân. |
| Natri polystyrene (Kayexalate) | Tăng kali máu liên quan đến suy thận hoặc do thuốc |
| Xét nghiệm cận lâm sàng |
| Thời gian hoạt hóa bán phần thromboplastin (aPTT) > 100 giây | Quá liều thuốc chống đông heparin |
| Giá trị INR1 > 6 | Quá liều thuốc chống đông kháng vitamin K |
| Số lượng bạch cầu < 3.000 bạch cầu/mm3 | Giảm bạch cầu trung tính do thuốc hoặc tình trạng bệnh |
| Số lượng tiểu cầu < 50.000 tiểu cầu/mm3 | Giảm tiểu cầu do thuốc hoặc tình trạng bệnh |
| Glucose máu < 2,78 mmol/l | Hạ đường huyết liên quan đến sử dụng insulin và các thuốc điều trị đái tháo đường |
| Tăng creatinin huyết thanh | Độc tính trên thận liên quan đến thuốc hoặc tình trạng bệnh |
| Kali máu > 6 mEq/L | Tăng kali máu do thuốc hoặc tình trạng bệnh |
| Kali máu < 3 mEq/L | Hạ kali máu do thuốc hoặc tình trạng bệnh |
| Natri máu < 130 mEq/L | Hạ natri máu do thuốc hoặc tình trạng bệnh |
| Dương tính vi khuẩn Clostridium difficile trong phân | Bội nhiễm liên quan đến sử dụng kháng sinh phổ rộng |
| Biểu hiện lâm sàng |
| An thần quá mức, hôn mê, ngã | Liên quan tới lạm dụng thuốc an thần |
| Phát ban da | Phản ứng có hại của thuốc |
| Dấu hiệu khác |
| Dừng thuốc đột ngột không rõ nguyên nhân trong quá trình điều trị | Phản ứng có hại của thuốc |
| Chuyển lên mức chăm sóc cao hơn | Phản ứng có hại của thuốc |
| Lọc máu cấp | Suy thận cấp do thuốc |
| Truyền máu hoặc sử dụng chế phẩm máu | Liên quan thuốc chống đông |
1 INR (international normalized ratio): chỉ số chuẩn hóa quốc tế. PHỤ LỤC 6. SƠ ĐỒ PHÂN LOẠI SAI SÓT LIÊN QUAN ĐẾN THUỐC
Phân loại sai sót liên quan đến thuốc theo NCC MERP và sơ đồ diễn tiến phân loại sai sót liên quan đến thuốc như sau:
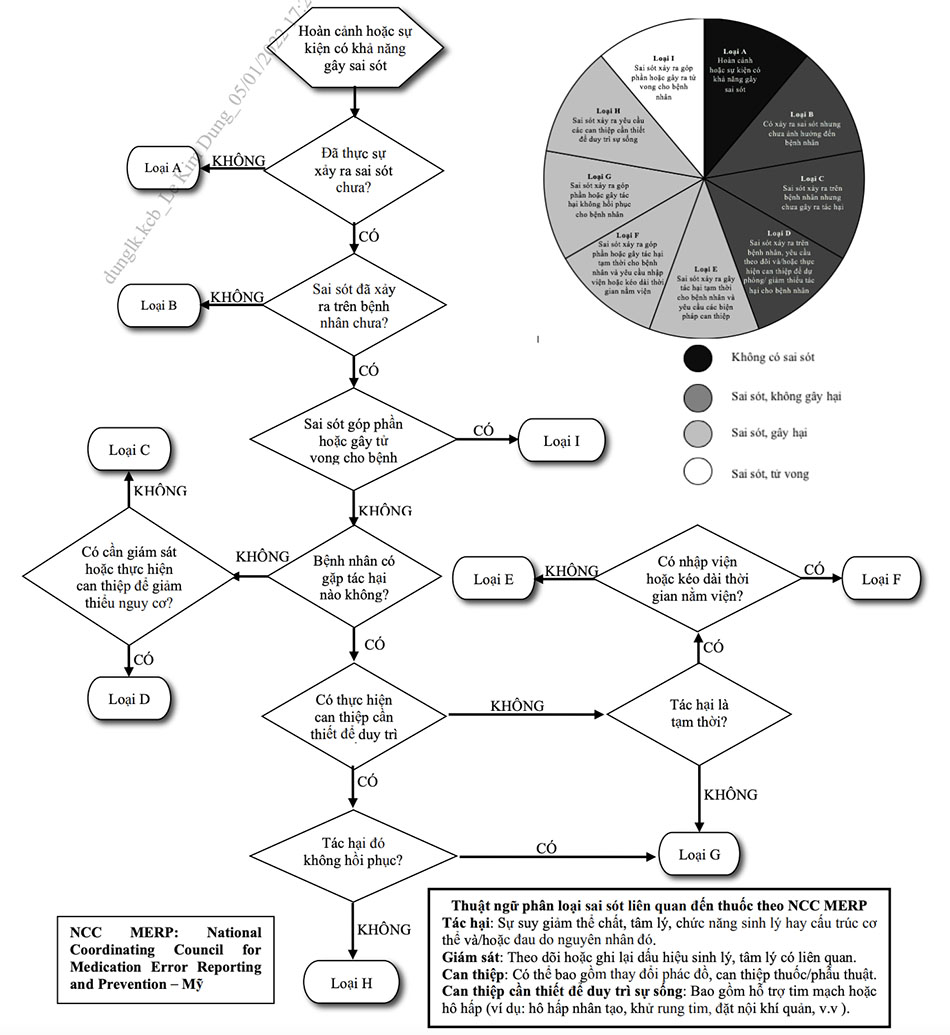
PHỤ LỤC 7. THANG ĐÁNH GIÁ MỐI LIÊN QUAN GIỮA THUỐC VÀ ADR
Một biến cố bất lợi xảy ra trong quá trình điều trị có thể có liên quan đến bệnh lý hoặc thuốc đang sử dụng của người bệnh. Việc xác định rõ nguyên nhân gây ra ADR là quy trình phức tạp, cần thu thập đầy đủ thông tin về người bệnh, về phản ứng có hại, về thuốc nghi ngờ và các thuốc dùng đồng thời. Khi xảy ra biến cố bất lợi cần xem xét đến khả năng liên quan đến thuốc bên cạnh các nguyên nhân khác. Tùy theo điều kiện chuyên môn, các cơ sở khám bệnh, chữa bệnh có thể đánh giá mối liên hệ giữa thuốc nghi ngờ và ADR theo thang phân loại của Tổ chức Y tế thế giới hoặc thang đánh giá của Naranjo để rút kinh nghiệm cho công tác chuyên môn. Đây là hai thang đánh giá được sử dụng phổ biến nhất hiện nay. Cần lưu ý, việc đánh giá này không bắt buộc khi báo cáo phản ứng có hại của thuốc. Nhân viên y tế, cơ sở khám bệnh, chữa bệnh cần gửi tất cả các báo cáo về ADR nghi ngờ do thuốc mà không cần kèm theo bất kỳ đánh giá nào. Các báo cáo sẽ được các chuyên gia của Trung tâm Quốc gia và Trung tâm khu vực thẩm định và gửi kết quả phản hồi cho người báo cáo và cơ sở khám bệnh, chữa bệnh trong trường hợp cần thiết.
1. Thang phân loại của Tổ chức Y tế thế giới (WHO)
Mối quan hệ giữa thuốc nghi ngờ và ADR được phân thành 6 mức độ (xem Bảng 7.1). Để xếp loại mối quan hệ giữa thuốc nghi ngờ và ADR ở mức độ nào, cần thỏa mãn tất cả các tiêu chuẩn đánh giá đã được quy định tương ứng với mức độ đó. Các cặp thuốc và ADR được phân loại ở các mức “chắc chắn”, “có khả năng” và “có thể” được đánh giá là có mối liên quan giữa thuốc nghi ngờ và ADR.
2. Thang đánh giá của Naranjo
Mối quan hệ giữa thuốc nghi ngờ và ADR được phân thành 4 mức bao gồm: chắc chắn, có khả năng, có thể, không chắc chắn. Thang đánh giá này đưa ra 10 câu hỏi (dựa trên các tiêu chí đánh giá biến cố bất lợi) và cho điểm dựa trên các câu trả lời (xem Bảng 7.2). Tổng điểm sẽ được sử dụng để phân loại mối quan hệ giữa thuốc nghi ngờ và ADR. Các cặp thuốc và ADR được phân loại ở các mức “chắc chắn”, “có khả năng” và “có thể” cũng được đánh giá là có mối liên quan giữa thuốc nghi ngờ và ADR. Bảng 7.1. Thang đánh giá mối quan hệ giữa thuốc nghi ngờ và ADR của WHO
| Quan hệ nhân quả | Tiêu chuẩn đánh giá |
| Chắc chắn (Certain) | · Phản ứng được mô tả (biểu hiện lâm sàng hoặc cận lâm sàng bất thường) có mối liên hệ chặt chẽ với thời gian sử dụng thuốc nghi ngờ, · Phản ứng xảy ra không thể giải thích bằng tình trạng bệnh lý của người bệnh hoặc các thuốc khác sử dụng đồng thời với thuốc nghi ngờ, · Các biểu hiện của phản ứng được cải thiện khi ngừng sử dụng thuốc nghi ngờ, · Phản ứng là tác dụng phụ đặc trưng đã được biết đến của thuốc nghi ngờ (có cơ chế dược lý rõ ràng) · Phản ứng lặp lại khi tái sử dụng thuốc nghi ngờ (nếu có dùng lại thuốc nghi ngờ). |
| Có khả năng (Probable/ likely) | · Phản ứng được mô tả có mối liên hệ hợp lý với thời gian sử dụng thuốc nghi ngờ, · Nguyên nhân gây ra phản ứng không chắc chắn được liệu có thể có liên quan đến bệnh lý của người bệnh hoặc các thuốc khác sử dụng đồng thời hay không, · Các biểu hiện của phản ứng được cải thiện khi ngừng sử dụng thuốc nghi ngờ, · Không cần thiết phải có thông tin về tái sử dụng thuốc. |
| Có thể (Possible) | · Phản ứng được mô tả có mối liên hệ hợp lý với thời gian sử dụng thuốc nghi ngờ, · Phản ứng có thể được giải thích bằng tình trạng bệnh lý của người bệnh hoặc các thuốc khác sử dụng đồng thời, · Thiếu thông tin về diễn biến của phản ứng khi ngừng sử dụng thuốc nghi ngờ hoặc thông tin về việc ngừng sử dụng thuốc không rõ ràng. |
| Không chắc chắn (Unlikely) | · Phản ứng được mô tả có mối liên hệ không rõ ràng với thời gian sử dụng thuốc, · Phản ứng có thể được giải thích bằng tình trạng bệnh lý của người bệnh hoặc các thuốc khác sử dụng đồng thời. |
| Chưa phân loại (Unclassified) | · Ghi nhận việc xảy ra phản ứng, nhưng cần thêm thông tin để đánh giá hoặc đang tiếp tục thu thập thông tin bổ sung để đánh giá. |
| Không thể phân loại (Unclassifiable) | · Ghi nhận phản ứng, nghi ngờ là phản ứng có hại của thuốc, nhưng không thể đánh giá được do thông tin trong báo cáo không đầy đủ hoặc không thống nhất, và không thể thu thập thêm thông tin bổ sung hoặc xác minh lại thông tin. |
Bảng 7.2. Thang đánh giá mối liên quan giữa thuốc nghi ngờ và ADR của Naranjo | STT | Câu hỏi đánh giá | Tính điểm | Điểm |
| Có | Không | Không có thông tin |
| 1 | Phản ứng có được mô tả trước đó trong y văn không? | 1 | 0 | 0 | |
| 2 | Phản ứng có xuất hiện sau khi điều trị bằng thuốc nghi ngờ không? | 2 | -1 | 0 | |
| 3 | Phản ứng có được cải thiện sau khi ngừng thuốc hoặc dùng chất đối kháng không? | 1 | 0 | 0 | |
| 4 | Phản ứng có tái xuất hiện khi dùng lại thuốc không? | 2 | -1 | 0 | |
| 5 | Có nguyên nhân nào khác (trừ thuốc nghi ngờ) có thể là nguyên nhân gây ra phản ứng hay không? | -1 | 2 | 0 | |
| 6 | Phản ứng có xuất hiện khi dùng giả dược (placebo) không? | -1 | 1 | 0 | |
| 7 | Nồng độ thuốc trong máu (hay các dịch sinh học khác) có ở ngưỡng gây độc không? | 1 | 0 | 0 | |
| 8 | Phản ứng có nghiêm trọng hơn khi tăng liều hoặc ít nghiêm trọng hơn khi giảm liều không? | 1 | 0 | 0 | |
| 9 | Người bệnh có gặp phản ứng tương tự với thuốc nghi ngờ hoặc các thuốc tương tự trước đó không? | 1 | 0 | 0 | |
| 10 | Phản ứng có được xác nhận bằng các bằng chứng khách quan như kết quả xét nghiệm bất thường hoặc kết quả chẩn đoán hình ảnh bất thường hay không? | 1 | 0 | 0 | |
| Tổng điểm | |
| Kết luận | |
Phần kết luận đánh số tương ứng với các mức phân loại sau:
- Chắc chắn ( ≥ 9 điểm).
- Có khả năng (5 – 8 điểm).
- Có thể (1 – 4 điểm).
- Nghi ngờ (<1 hoặc 0 điểm).
PHỤ LỤC 8. THANG ĐÁNH GIÁ KHẢ NĂNG PHÒNG TRÁNH ĐƯỢC CỦA ADR
Trên thực tế, ước tính có khoảng 10%-80% tổng số ADR là có thể “phòng tránh được”. Đáng chú ý, chi phí tổn thất do ADR có thể phòng tránh được cao hơn so với những ADR không phòng tránh được. Vì vậy, nếu giảm thiểu được tỷ lệ ADR có thể phòng tránh được sẽ giúp giảm thiểu đáng kể hậu quả và gánh nặng của ADR. Các ADR “phòng tránh được” phản ánh các vấn đề liên quan đến thuốc có thể gây tổn thương thực sự trên người bệnh. Do đó, nhân viên y tế (đặc biệt là các dược sĩ lâm sàng) cần được trang bị các kỹ năng cần thiết và được đào tạo phù hợp nhằm phát hiện các ADR phòng tránh được để phát hiện các vấn đề tiềm tàng liên quan đến thuốc. Một số phương pháp đã được xây dựng để đánh giá khả năng “phòng tránh được” của ADR, tuy nhiên chưa có phương pháp "chuẩn vàng" trong lĩnh vực này. 1. Phương pháp P đề xuất bởi nhóm chuyên gia của WHO
Phương pháp P được áp dụng để phát hiện một cách hệ thống các sai sót liên quan đến thuốc trong các báo cáo ca đơn lẻ về an toàn thuốc, có thể áp dụng được cho bất kỳ biến cố bất lợi nào sau khi xác định được quan hệ nhân quả giữa biến cố và thuốc nghi ngờ. Mục đích của phương pháp P không phải để phân loại các sai sót liên quan đến thuốc hay thực hiện phân tích nguyên nhân gốc rễ. Các tài liệu tham chiếu khuyến cáo nên được sử dụng trong đánh giá ca bao gồm tờ hướng dẫn sử dụng thuốc, các hướng dẫn điều trị của Bộ Y tế, của các hiệp hội trong nước và trên thế giới, và các tài liệu tham chiếu tương tự khi đánh giá khả năng phòng tránh được của ADR - Phương pháp P yêu cầu câu trả lời “có”, “không”, “không áp dụng được” hoặc “không rõ” với từng câu hỏi của tất cả 20 tiêu chí với mỗi ADR (xem Bảng 8.1). Câu trả lời “có” cho bất kỳ tiêu chí nào được coi là ADR xảy ra có thể “phòng tránh được”. Điều này gợi ý nguyên nhân gây ra ADR, từ đó xác định các tiêu chí quan trọng liên quan đến khả năng xảy ra ADR. Các tiêu chí quan trọng này thay đổi tùy thuộc vào nguyên nhân gây ADR: - Nếu nguyên nhân gây ADR liên quan đến liều dùng, các tiêu chí quan trọng cần được khai thác bao gồm tiêu chí 1, 2, 3, 4, 9, 10, 12, 13 và 16.
- Nếu ADR liên quan đến yếu tố thời gian, các tiêu chí quan trọng là 3, 4, 7 và 15.
- Tiêu chí 9, 10 và 11 là các tiêu chí quan trọng với ADR liên quan đến tính nhạy cảm với thuốc của người bệnh.
- Hành vi của người bệnh và chất lượng thuốc nên được khai thác một cách hệ thống vì những yếu tố này có thể làm tăng khả năng xuất hiện bất cứ ADR nào (tiêu chí 5, 6, 17, 18, 19, 20).
- Một tiêu chí được xem là "không áp dụng được" nếu như không có mối liên hệ (ví dụ: việc kê đơn 2 thuốc có cùng thành phần không ảnh hưởng đến khả năng xảy ra dị ứng thuốc). - Kết quả đánh giá sẽ rơi vào 1 trong 3 trường hợp: "có thể phòng tránh được", "không thể phòng tránh được" và "không đánh giá được".
- ADR được coi là “phòng tránh được” khi xác định được ít nhất 1 tiêu chí quan trọng.
- ADR được coi là “không phòng tránh được” nếu không có tiêu chí quan trọng nào được xác định từ báo cáo ca đơn lẻ về an toàn thuốc.
- Trường hợp được phân loại "không đánh giá được" nếu không có hoặc không đủ dữ liệu cần thiết để đánh giá. Ví dụ: phản vệ do kháng sinh nhóm penicillin được cho là "không đánh giá được" nếu không có thông tin khai thác về tiền sử dị ứng thuốc trước đó của người bệnh, hoặc trong những tình huống còn tranh cãi (ví dụ: một thuốc không được phê duyệt chính thức cho chỉ định trong nhi khoa nhưng thường xuyên được sử dụng cho trẻ em).
2. Phương pháp của mạng lưới các trung tâm Cảnh giác Dược Pháp
- Khả năng phòng tránh được của ADR được đánh giá bằng cách chọn câu trả lời và cho điểm cho từng mục theo các câu hỏi trong bộ tiêu chí (xem Bảng 8.2). Các tiêu chí đánh giá được phân loại theo hai mục, lần lượt là:
- Phát hiện các sai sót trong quy trình sử dụng thuốc (sai sót trong quá trình sản xuất, cấp phát, kê đơn, sử dụng, dịch đơn, tự ý sử dụng thuốc kê đơn và vấn đề trong tuân thủ);
- Đánh giá tính phù hợp của việc sử dụng thuốc trên người bệnh (phù hợp với khuyến cáo, các yếu tố nguy cơ, hoàn cảnh sống và tình trạng bệnh lý của người bệnh). Mỗi phương án trả lời sẽ được quy đổi thành điểm số.
- Khả năng phòng tránh được của ADR được phân loại theo 4 mức độ dựa trên sai sót phát hiện được hoặc điểm tổng của từng thuốc nghi ngờ được đánh giá, gồm có: “phòng tránh được” (-13 đến -8), “có khả năng phòng tránh được” (-7 đến -3), “không đánh giá được” (-2 đến 2) và “không phòng tránh được” (+3 đến +8). - Thang đánh giá khả năng phòng tránh được của Pháp đã được sử dụng trong nhiều nghiên cứu khác nhau trên nhiều nhóm thuốc và đối tượng khác nhau. Các nghiên cứu đã chỉ ra trong nhiều trường hợp, không có hoặc thiếu thông tin để trả lời cho một hay nhiều tiêu chí đánh giá khiến việc cho điểm có thể chưa được chính xác. Một số thông tin thường không khai thác được đầy đủ để đánh giá về tương tác thuốc, tính ưu tiên lựa chọn thuốc trên lâm sàng hoặc điều kiện sống của người bệnh. Vì vậy, khó có thể xác định được tính hợp lý tuyệt đối của một chỉ định. Bên cạnh đó, tính thống nhất và toàn diện của các tài liệu tham chiếu như tờ thông tin sản phẩm, hướng dẫn điều trị hay các tài liệu khác cũng là một yếu tố ảnh hưởng. Những hạn chế này dẫn đến tính đồng thuận giữa các chuyên gia khi đánh giá là không cao. - Bên cạnh một số mặt hạn chế về thông tin cho đánh giá giống như nhiều bộ công cụ khác, những tiêu chí trong thang đánh giá của Pháp cho thấy phương pháp này không chỉ chú trọng các sai sót hay tính thiếu tuân thủ khuyến cáo, mà còn quan tâm đến việc tối ưu hóa điều trị ở người bệnh. Do đó, thang đánh giá pADR của Pháp có ý nghĩa cao về mặt lâm sàng. Đồng thời, so với phương pháp P của WHO với 20 tiêu chí, mà một số tiêu chí trong đó thường không đánh giá được, phương pháp của Pháp đơn giản hơn, đòi hỏi ít thời gian để đánh giá hơn. Bảng 8.1. Bảng đánh giá khả năng phòng tránh được của ADR (theo phương pháp P của Tổ chức Y tế Thế giới)
| Các yếu tố liên quan | Các tiêu chí về khả năng phòng tránh được | Có | Không | Không rõ | Không áp dụng |
| Thực hành chuyên môn "Pr" | 1. Liều không phù hợp? | | | | |
| 2. Đường dùng không phù hợp? | | | | |
| 3. Thời gian sử dụng thuốc không phù hợp? | | | | |
| 4. Sử dụng dạng thuốc không phù hợp? | | | | |
| 5. Sử dụng thuốc hết hạn? | | | | |
| 6. Bảo quản thuốc không phù hợp? | | | | |
| 7. Cách dùng không phù hợp (thời gian, tốc độ, tần suất, kỹ thuật, pha chế, thao tác, trộn lẫn)? | | | | |
| 8. Chỉ định không phù hợp? | | | | |
| 9. Không phù hợp với đặc điểm của người bệnh (tuổi, giới, phụ nữ mang thai, khác)? | | | | |
| 10. Không phù hợp với tình trạng lâm sàng (suy thận, suy gan…) hoặc bệnh lý đang có của người bệnh? | | | | |
| 11. Có tiền sử quá mẫn với thuốc hoặc các thuốc khác trong nhóm? | | | | |
| 12. Tương tác thuốc-thuốc? | | | | |
| 13. Trùng lặp điều trị (kê đơn 2 hay nhiều thuốc có thành phần tương tự nhau)? | | | | |
| 14. Không sử dụng thuốc cần dùng? | | | | |
| 15. Hội chứng cai thuốc (do ngừng thuốc đột ngột)? | | | | |
| 16. Xét nghiệm hoặc theo dõi lâm sàng không phù hợp? | | | | |
| Chế phẩm/ thuốc "Pd" | 17. Đã sử dụng thuốc nghi ngờ kém chất lượng? | | | | |
| 18. Đã sử dụng thuốc nghi ngờ là giả? | | | | |
| Người bệnh "Pa" | 19. Không tuân thủ điều trị? | | | | |
| 20. Người bệnh tự ý dùng thuốc kê đơn? | | | | |
Bảng 8.2. Bảng đánh giá khả năng phòng tránh được của ADR (theo phương pháp của mạng lưới các Trung tâm Cảnh giác Dược Pháp)
 b
b Khuyến cáo sử dụng thuốc cập nhật nhất, có thể tiếp cận được tính đến ngày cuối cùng kê đơn hay dùng thuốc của người bệnh. Nguồn khuyến cáo gồm có ít nhất 01 trong số các tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc được phê duyệt tại Việt Nam hoặc một số nước tham chiếu khác, hoặc Hướng dẫn chẩn đoán và điều trị được Bộ Y tế ban hành.
a ADR được ghi nhận ở ít nhất 01 tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc (Anh/Hoa Kỳ/Pháp), Micromedex hoặc Hướng dẫn điều trị.
c 1- Phòng tránh được (-13 đến -8 hoặc phát hiện được ít nhất 1 sai sót trong quy trình sử dụng thuốc); 2 – Có khả năng phòng tránh được (-7 đến -3) ; 3- Không đánh giá được (-2 đến 2) ; 4 – Không phòng tránh được (+3 đến +8).
PHỤ LỤC 9. THANG ĐÁNH GIÁ CHẤT LƯỢNG CỦA BÁO CÁO ADR
Chất lượng báo cáo được đánh giá dựa trên cách tính điểm hoàn thành báo cáo (report completeness score) theo thang điểm VigiGrade của Trung tâm theo dõi Uppsala - Tổ chức Y tế thế giới WHO (Trung tâm WHO–UMC). + Điểm hoàn thành một báo cáo được tính bằng trung bình cộng điểm của các cặp thuốc – ADR trong báo cáo, với điểm hoàn thành báo cáo của một cặp thuốc – ADR được tính theo công thức:
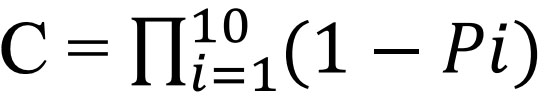
Trong đó: C là điểm hoàn thành của một cặp thuốc – ADR Pi là điểm phạt của mỗi trường thông tin bị thiếu (
xem Bảng 9.1) + Các báo cáo không có thông tin về thuốc nghi ngờ và/hoặc không mô tả biểu hiện ADR được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). + Điểm hoàn thành của một báo cáo thấp nhất là 0 và cao nhất là 1. Báo cáo có điểm hoàn thành < 0,8 là báo cáo kém chất lượng và báo cáo có điểm hoàn thành từ 0,8 đến 1 điểm là báo cáo chất lượng tốt.
Bảng 9.1. Điểm phạt các trường thông tin trong báo cáo ADR theo thang điểm VigiGrade 2 | Trường thông tin | Mô tả | Yêu cầu | Điểm phạt (Pi) |
| Loại báo cáo | Loại báo cáo (báo cáo tự nguyện, báo cáo từ các nghiên cứu) | § Nếu không nêu rõ loại báo cáo: trừ 10% số điểm § Nếu gửi báo cáo theo mẫu ban hành kèm theo Thông tư số 23/2011/TT-BYT ngày 10/06/2011, được coi là báo cáo tự nguyện | 10% |
| Người báo cáo | Thông tin về chức vụ của người báo cáo. | § Chức vụ của người báo cáo có thể là: bác sỹ (trưởng khoa, phó khoa), dược sỹ (dược sỹ đại học, dược sỹ trung học, trưởng khoa dược, phó khoa dược), điều dưỡng, hộ sinh viên, điều dưỡng, y sỹ, nhân viên y tế khác (cán bộ, nhân viên thống kê …). § Trong trường hợp không điền hoặc chức vụ không phù hợp (không phải là nhân viên y tế trong bệnh viện): trừ 10% số điểm | 10% |
2
Trong trường hợp báo cáo không có thông tin về thuốc nghi ngờ và không có mô tả về ADR thì được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). | Trường thông tin | Mô tả | Yêu cầu | Điểm phạt (Pi) |
| Giới tính | Giới tính của người bệnh | § Nếu bỏ trống: trừ 30% số điểm | 30% |
| Thời gian tiềm tàng xuất hiện ADR | Thời gian xảy ra ADR | § Mục 5 (ngày xuất hiện phản ứng) có thể được thay thế bằng ngày kết thúc sử dụng thuốc. Nếu không có thông tin này: trừ 50% số điểm. § Nếu có ngày xuất hiện phản ứng mà thiếu thông tin về ngày bắt đầu sử dụng thuốc hoặc thông tin này không phù hợp (sau ngày xuất hiện phản ứng): trừ 50% số điểm. § Nếu có ngày xuất hiện phản ứng và chỉ có thông tin về tháng bắt đầu sử dụng thuốc: trừ 10% số điểm. § Nếu có ngày xuất hiện phản ứng và chỉ có thông tin về năm bắt đầu sử dụng thuốc: trừ 30% số điểm. | 50% |
| Tuổi của người bệnh | Năm sinh hoặc tuổi của người bệnh | § Nếu không điền mục này: trừ 30% số điểm. § Nếu chỉ điền nhóm tuổi: trừ 10% số điểm. § Yêu cầu tuổi của người bệnh nằm trong khoảng từ 0-134. | 30% |
| Diễn biến của phản ứng | Hậu quả của ADR | § Không điền cả 3 mục 12 (kết quả sau xử trí phản ứng), 14 (kết quả sau khi ngừng/giảm liều), 15 (kết quả sau khi tái sử dụng thuốc) trừ 30% số điểm. § Điền đủ cả 3 mục nhưng thông tin thu được mâu thuẫn: trừ 30% số điểm. | 30% |
| Lý do sử dụng thuốc | Chỉ định của thuốc nghi ngờ | § Nếu không điền hoặc chỉ định của thuốc không rõ ràng: trừ 30% số điểm. | 30% |
| Liều dùng | Lượng thuốc sử dụng trong ngày | § Nếu thiếu 1 trong 2 mục liều sử dụng một lần và số lần dùng trong ngày: trừ 10% số điểm. | 10% |
| Thông tin bổ sung | Thông tin bổ sung | § Không điền cả 4 mục 8 (các xét nghiệm liên quan đến phản ứng), 9 (tiền sử), 10 (cách xử trí phản ứng), 19 (bình luận của nhân viên y tế) trừ 10% số điểm | 10% |
| Khoa/phòng, bệnh viện | Khoa/phòng, bệnh viện | § Tên Khoa/phòng, cơ sở khám bệnh, chữa bệnh. | 10% |
PHỤ LỤC 10. NHỮNG ĐIỂM CẦN LƯU Ý TRONG QUÁ TRÌNH SỬ DỤNG THUỐC ĐỂ GIẢM THIỂU KHẢ NĂNG XUẤT HIỆN ADR
Trong quá trình kê đơn, cấp phát thuốc hoặc thực hiện y lệnh, nhân viên y tế cần cân nhắc các yếu tố sau:
- Thuốc có phù hợp với tình trạng lâm sàng của người bệnh không?
- Liều dùng, đường dùng và khoảng cách giữa các lần đưa thuốc có hợp lý không?
- Đã làm các xét nghiệm cận lâm sàng liên quan và đánh giá kết quả các xét nghiệm này chưa?
- Tình trạng bệnh lý người bệnh có khả năng ảnh hưởng tới dược động học của thuốc không?
- Người bệnh có tiền sử dị ứng với thuốc hoặc các thuốc khác trong cùng nhóm dược lý hay không?
- Người bệnh có đang dùng thuốc khác (hoặc thuốc y học cổ truyền) có khả năng gây tương tác thuốc hay không?
- Thuốc được kê đơn có phải là thuốc có nguy cơ cao gây ra ADR không? (Ví dụ: kháng sinh nhóm aminoglycosid, digoxin, thuốc chống đông kháng vitamin K, heparin, hóa trị liệu điều trị ung thư) hay các thuốc cần thận trọng tăng cường theo dõi người bệnh hoặc thường xuyên làm các xét nghiệm theo dõi không? (Ví dụ: công thức máu, điện giải đồ, creatinin huyết thanh, xét nghiệm chức năng gan, xét nghiệm chức năng đông máu…).
- Thuốc đã hết hạn sử dụng chưa? Thuốc có được bảo quản đúng theo yêu cầu không? (với các thuốc cần điều kiện bảo quản đặc biệt).
- Về quan sát cảm quan, có thấy dấu hiệu bất thường nào về chất lượng không? (Ví dụ: đổi màu, mất màu thuốc…).
- Các thiết bị, dụng cụ tiêm truyền có vô trùng hay không?
Chú ý: - Không kê đơn thuốc nếu không có lý do rõ ràng giải thích cho việc kê đơn thuốc đó.
- Thận trọng khi kê đơn và sử dụng thuốc cho bệnh nhân nhi, người bệnh cao tuổi, phụ nữ có thai hoặc đang cho con bú, người bệnh nặng, người bệnh suy giảm chức năng gan, thận. Theo dõi chặt chẽ những người bệnh này trong quá trình sử dụng thuốc.
- Thận trọng khi kê đơn những thuốc được biết đến là có nguy cơ cao gây phản ứng có hại và tương tác thuốc (thuốc chống đông, thuốc hạ đường huyết, các thuốc tác dụng trên hệ thần kinh trung ương…); giám sát chặt chẽ những người bệnh đã có biểu hiện ADR khi dùng thuốc.
- Thận trọng về tương tác giữa thuốc với thức ăn, rượu và đồ uống khác.
- Tránh những phối hợp thuốc không cần thiết.
- Xem xét toàn bộ các thuốc mà người bệnh đã sử dụng, bao gồm cả các thuốc không kê đơn, thuốc dược liệu, thuốc y học cổ truyền.
- Nếu người bệnh có những biểu hiện hoặc triệu chứng bất thường không rõ có liên quan đến tình trạng bệnh lý hay không, cân nhắc đến khả năng xảy ra phản ứng có hại của thuốc.
- Khi nghi ngờ phản ứng có hại đã xảy ra trên người bệnh, cân nhắc giảm liều hoặc ngừng thuốc nghi ngờ càng sớm càng tốt, xử trí, đánh giá và báo cáo ADR của thuốc đó.
PHỤ LỤC 11. DANH SÁCH MỘT SỐ ĐỐI TƯỢNG NGƯỜI BỆNH VÀ THUỐC CÓ NGUY CƠ CAO XUẤT HIỆN ADR
1. Một số đối tượng có nguy cơ cao xảy ra ADR
- Người bệnh có tiền sử gặp ADR, dị ứng thuốc. - Người bệnh có yếu tố cơ địa suy giảm miễn dịch hoặc mắc các bệnh tự miễn. - Người bệnh mắc đồng thời nhiều bệnh. - Người bệnh sử dụng nhiều thuốc. - Người bệnh sử dụng thuốc kéo dài. - Người bệnh có rối loạn chức năng gan, thận. - Người bệnh cao tuổi, bệnh nhi. - Người nghiện rượu. - Phụ nữ mang thai, cho con bú. - Người bệnh được điều trị bằng các thuốc có nguy cơ cao xảy ra phản ứng có hại. - Người bệnh sử dụng thuốc được biết đến có liên quan đến các biến cố bất lợi nghiêm trọng. - Người bệnh được điều trị bằng các thuốc có phạm vi điều trị hẹp hoặc tiềm ẩn nhiều tương tác thuốc nghiêm trọng. - Người bệnh có chỉ số xét nghiệm cận lâm sàng bất thường. - Người bệnh được chỉ định sử dụng 1 liều thuốc kháng histamin, adrenalin hoặc corticosteroid (là dấu hiệu có thể xuất hiện phản ứng có hại). 2. Một số thuốc có nguy cơ cao gây ADR (theo phân loại của ISMP)
a. Nhóm thuốc
- Thuốc chủ vận adrenergic, dùng đường tiêm tĩnh mạch (ví dụ: adrenalin, phenylephrin, noradrenalin, dopamin, dobutamin). - Thuốc chẹn β adrenergic, dùng đường tiêm tĩnh mạch (ví dụ: propanolol, metoprolol, labetalol). - Thuốc mê hô hấp và thuốc mê tĩnh mạch (ví dụ: propofol, ketamin). - Thuốc chống loạn nhịp, dùng đường tiêm tĩnh mạch (ví dụ: lidocain, amiodaron). - Thuốc chống đông kháng vitamin K, heparin khối lượng phân tử thấp, heparin không phân đoạn tiêm tĩnh mạch, thuốc ức chế yếu tố Xa (fondaparinux), thuốc ức chế trực tiếp thrombin (ví dụ: argatroban, lepiridin, bivalirudin), thuốc tiêu sợi huyết (ví dụ: alteplase, reteplase, tenecteplase) và thuốc chống kết tập tiểu cầu ức chế thụ thể glycoprotein IIb/IIIa (ví dụ: eptifibatid). - Dung dịch làm liệt cơ tim. - Hóa trị liệu sử dụng trong điều trị ung thư, dùng đường tiêm hoặc uống. - Dextrose, dung dịch ưu trương (nồng độ ≥ 20%). - Dung dịch lọc máu trong thẩm phân phúc mạc hoặc chạy thận nhân tạo. - Thuốc gây tê ngoài màng cứng (ví dụ: bupivacain). - Insulin, dùng tiêm dưới da và tiêm tĩnh mạch. - Thuốc tăng co bóp cơ tim, dùng đường tiêm tĩnh mạch (ví dụ: digoxin, milrinon). - Thuốc được bào chế dạng liposom và dạng bào chế quy ước tương ứng (ví dụ: amphotericin B dạng liposom và amphotericin B deoxycholat). - Thuốc an thần, dùng đường tiêm tĩnh mạch (ví dụ: midazolam, lorazepam). - Thuốc an thần, dùng đường uống, cho trẻ em (ví dụ: cloral hyrat, midazolam). - Opioid dùng trong gây mê hoặc giảm đau, dùng đường tiêm tĩnh mạch, hệ trị liệu qua da hoặc dùng đường uống. - Thuốc phong bế dẫn truyền thần kinh, cơ (ví dụ: succinylcholin, rocuronium, vecuronium). - Thuốc cản quang, dùng đường tiêm. - Chế phẩm nuôi dưỡng ngoài đường tiêu hóa. - Natri clorid, dùng đường tiêm, dung dịch ưu trương (nồng độ > 0,9%). - Nước vô khuẩn để truyền, khí dung và rửa vết thương (không bao gồm dạng chai rót) có thể tích từ 100 mL trở lên. - Thuốc điều tri đái tháo đường nhóm sulfonylurea, dùng đường uống (ví dụ: glimepirid, glyburid, glipizid). b. Các thuốc cụ thể
- Adrenalin, dùng đường tiêm dưới da. - Epoprostenol, dùng đường tiêm tĩnh mạch. - Insulin U-500 (đặc biệt lưu ý). - Magie sulfat, dùng đường tiêm. - Methotrexat dùng đường uống được sử dụng với chỉ định không phải điều trị ung thư. - Oxytocin, dùng đường tiêm tĩnh mạch. - Natri nitroprussid, dùng đường tiêm. - Kali clorid dung dịch đậm đặc, dùng đường tiêm. - Kali phosphat, dùng đường tiêm. - Promethazin, dùng đường tiêm tĩnh mạch. - Vasopressin dùng đường tiêm tĩnh mạch hoặc tiêm trong xương. - Dẫn chất alkaloid Dừa cạn (vinblastin, vinorelbin, vincristin), dùng đường tiêm. PHỤ LỤC 12. HƯỚNG DẪN QUẢN LÝ THUỐC CÓ NGUY CƠ CAO
1. Phân loại thuốc có nguy cơ cao
Tham khảo bảng phân loại APINCHS sau để xây dựng danh mục thuốc có nguy cơ cao tại cơ sở khám bệnh, chữa bệnh. Bảng phân loại này không đề cập đầy đủ hết các thuốc có nguy cơ cao, tuỳ theo đặc điểm sử dụng thuốc và đặc điểm bệnh nhân điều trị, cơ sở khám bệnh, chữa bệnh cần lựa chọn các thuốc có nguy cơ cao phù hợp để đưa vào danh mục. Bảng 12.1. Phân loại thuốc có nguy cơ cao theo APINCHS (phân loại của Úc). | Phân loại | Ví dụ |
| A | Kháng sinh | Aminoglycosid: gentamicin, tobramycin và amikacin Vancomycin Amphotericin – dạng liposom |
| P | Kali và chất điện giải | Các chất điện giải đậm đặc sử dụng đường tiêm: kali, magie, calci, natri clorid ưu trương |
| I | Insulin | Tất cả các loại insulin |
| N | Thuốc giảm đau opioid và thuốc an thần khác | Hydromorphon, oxycodon, morphin, fentanyl, alfentanil, remfentanil Benzodiazepin: diazepam, midazolam Thiopenton, propofol và các thuốc gây mê tác dụng ngắn |
| C | Hóa trị liệu | Vincristin, methotrexat, etoposid, azathioprin Thuốc hóa trị đường uống |
| H | Heparin và các thuốc chống đông máu | Heparin và heparin khối lượng phân tử thấp (LMWH): dalteparin, enoxaparin, warfarin Thuốc chống đông đường uống tác dụng trực tiếp (DOAC): dabigatran, rivaroxaban, apixaban |
| S | Hệ thống | Hệ thống an toàn thuốc như kiểm tra 2 lần độc lập, an toàn đường dùng với các thuốc dạng dung dịch… |
2. Một số yêu cầu đảm bảo an toàn khi thực hành sử dụng thuốc có nguy cơ cao
a) Miếng dán qua da - Cần có xác nhận của bác sĩ kê đơn nếu phải sử dụng nhiều miếng dán ngoài da. - Thời gian sử dụng, vị trí dùng và thời điểm gỡ miếng dán cần được ghi trong đơn thuốc. - Không nên để các miếng dán thẩm thấu qua da tiếp xúc với nhiệt độ quá cao. - Không nên cắt miếng dán. - Các miếng dán thẩm thấu qua da có chứa opioid nên được vứt bỏ một cách an toàn (ví dụ: bỏ vào thùng đựng vật sắc nhọn). b) Thuốc uống dạng giải phóng kéo dài - Các dạng bào chế này không được hòa tan, chia nhỏ (trừ khi đã cho phép trước đó) hoặc nghiền nhỏ trước khi sử dụng. - Cần liên hệ với khoa Dược để được tư vấn về dạng bào chế hoặc liều dùng thay thế nếu người bệnh khó nuốt. c) Thuốc hít sử dụng qua các thiết bị - Đảm bảo người bệnh hiểu và có thể sử dụng các thiết bị một cách chính xác. - Đảm bảo cài đặt thiết bị chính xác cho mỗi lần sử dụng thuốc. - Đảm bảo sử dụng thuốc đúng dạng và hàm lượng. d) Dung dịch tiêm - Nếu điều kiện cung ứng thuốc cho phép, các loại thuốc nguy cơ cao trong danh mục thuốc nên tương đồng nhất về độ pha loãng và hàm lượng được dùng điều trị để giảm thiểu tối đa nguy cơ sai sót trong quá trình chuẩn bị. Ưu tiên sử dụng dịch truyền pha sẵn có thể sử dụng ngay với các thuốc nguy cơ cao. - Cần có chỉ định rõ ràng và ghi hướng dẫn chi tiết vào phiếu chăm sóc của người bệnh nếu cần thiết phải thay đổi hàm lượng dịch truyền đã pha sẵn. 3. Ví dụ hướng dẫn quản lý một số thuốc/nhóm thuốc có nguy cơ cao
3.1. Thuốc chống đông
Thuốc chống đông có khoảng điều trị hẹp và khi dùng quá liều hoặc dưới liều điều trị có thể gây ra các phản ứng có hại nghiêm trọng cho người bệnh. Các sai sót liên quan đến thuốc chống đông có thể bao gồm: - - Trùng lặp điều trị (ví dụ: sử dụng thuốc dự phòng thuyên tắc huyết khối tĩnh mạch (VTE) cho người bệnh đang điều trị bằng các thuốc chống đông).
- - Sử dụng liều điều trị khi đã dùng liều dự phòng và ngược lại.
- - Chưa hiệu chỉnh liều theo đặc điểm người bệnh (ví dụ: kết quả xét nghiệm huyết học, mức lọc cầu thận, tuổi và cân nặng).
- - Chưa thực hiện đúng hướng dẫn (ví dụ: đường dùng của dung dịch heparin không phân đoạn không đúng theo hướng dẫn dẫn đến liều sử dụng không chính xác).
- - Sử dụng không đúng hướng dẫn sau khi xuất viện (ví dụ: chưa thông tin đầy đủ về việc dùng thuốc chống đông tới người bệnh và/hoặc người chăm sóc sau khi người bệnh xuất viện dẫn đến xảy ra phản ứng có hại của thuốc).
Hướng dẫn dưới đây gợi ý các thao tác tối thiểu cần thiết để giảm thiểu các nguy cơ liên quan đến việc sử dụng thuốc chống đông. Hướng dẫn này không bao gồm hướng dẫn lâm sàng về việc sử dụng thuốc chống đông. a) Chiến lược giảm thiểu nguy cơ
Hướng dẫn của Hội đồng Thuốc và điều trị tại cơ sở khám bệnh, chữa bệnh phải bao gồm các thuốc chống đông sau đây: heparin không phân đoạn, warfarin, heparin trọng lượng phân tử thấp và thuốc chống đông đường uống không kháng vitamin K (NOAC). Hội đồng Thuốc và điều trị của bệnh viện nên phê duyệt các hướng dẫn sử dụng thuốc trong đó chứa các thông tin sau: - Yêu cầu ghi lại cân nặng người bệnh đối với tất cả người bệnh đang điều trị chống đông. - Hướng dẫn ước tính mức lọc cầu thận của người bệnh. - Hướng dẫn dùng liều dựa trên bằng chứng và hướng dẫn kê đơn (xem mục c-Kê đơn). - Quản lý thuốc chống đông ở người bệnh: - Chống chỉ định tuyệt đối hoặc tương đối với các thuốc chống đông.
- Có tiền sử các vấn đề đông máu (ví dụ: chảy máu, giảm tiểu cầu do heparin (HIT)).
- Có nguy cơ chảy máu (ví dụ: có kế hoạch phẫu thuật, rối loạn chức năng tiểu cầu).
- Phụ nữ có thai hoặc đang cho con bú.
- Theo dõi và xử trí giảm tiểu cầu do heparin. - Theo dõi tình trạng giảm tiểu cầu hoặc bất kỳ huyết khối mới hoặc kéo dài ở những người bệnh đang dùng hoặc gần đây đã ngừng dùng heparin. - Xử trí chảy máu ở người bệnh dùng thuốc chống đông bao gồm cả giai đoạn chuyển viện, chuyển tuyến. - Hướng dẫn chuyển đổi giữa các loại thuốc chống đông khác nhau. - Hướng dẫn hoặc tham khảo các hướng dẫn để quản lý thuốc chống đông trong thời gian phẫu thuật bao gồm: - Các trường hợp chỉ định liệu pháp chống đông bắc cầu.
- Thời gian ngừng và bắt đầu lại thuốc chống đông (nếu cần).
- Xử trí phẫu thuật đối với người bệnh đang sử dụng thuốc chống kết tập tiểu cầu.
- Thời gian gây tê vùng não-tủy sống và gây tê tại chỗ, cũng như rút dẫn lưu, dẫn lưu não thất ở người bệnh đang điều trị chống đông.
- Cần phải xem xét cụ thể đối với từng cá thể người bệnh về nguy cơ chảy máu trong khi làm thủ thuật.
- Tổ chức các chương trình đào tạo cụ thể cập nhật kiến thức và kỹ năng liên quan đến kê đơn hoặc quản lý sử dụng thuốc chống đông. - Tư vấn, giáo dục người bệnh và/hoặc người chăm sóc (xem mục Tư vấn/giáo dục cho người bệnh) về sử dụng thuốc chống đông an toàn. b) Yêu cầu hướng dẫn bổ sung với các thuốc chống đông cụ thể sau:
❖ Heparin không phân đoạn tiêm tĩnh mạch Trong điều kiện cho phép, nên chuẩn hóa Hướng dẫn sử dụng heparin không phân đoạn tiêm tĩnh mạch tại các cơ sở khám bệnh, chữa bệnh. Trong trường hợp không thể chuẩn hóa, Hướng dẫn phải đảm bảo giảm thiểu được các nguy cơ liên quan đến việc chuyển người bệnh trong và giữa các cơ sở khám bệnh, chữa bệnh. Hội đồng Thuốc và điều trị của bệnh viện nên xây dựng và ban hành Hướng dẫn của bệnh viện bao gồm các nội dung sau: - Chỉ định thuốc heparin không phân đoạn tiêm tĩnh mạch. - Các khoa lâm sàng có thể sử dụng heparin không phân đoạn tiêm tĩnh mạch. - Hướng dẫn cách tính liều heparin không phân đoạn, bao gồm ưu tiên sử dụng cân nặng thực tế, cân nặng lý tưởng hoặc cân nặng hiệu chỉnh của người bệnh để tính liều. - Khuyến cáo sử dụng liều nạp heparin tuỳ theo chỉ định. - Ghi rõ liều và tốc độ truyền tương ứng tuỳ theo chỉ định. - Theo dõi tình trạng đông máu. - Phạm vi điều trị cho thời gian hoạt hóa bán phần thromboplastin (aPTT) (tham khảo ý kiến của khoa xét nghiệm). - Hướng dẫn hiệu chỉnh liều dựa trên kết quả aPTT. - Các biện pháp xử trí đảo ngược tác dụng chống đông trong trường hợp quá liều. ❖ Thuốc chống đông kháng vitamin K Hội đồng Thuốc và điều trị của bệnh viện nên xây dựng và ban hành Hướng dẫn của bệnh viện bao gồm các nội dung sau: - Hướng dẫn về liều dùng, có cân nhắc đến: - Yếu tố nguy cơ chảy máu.
- Tuổi.
- Kết quả INR.
- Các bệnh lý hoặc tình trạng bệnh đang có suy tim, bệnh gan, nhiễm trùng nặng, vừa trải qua phẫu thuật lớn, giảm hấp thu qua đường tiêu hóa, suy dinh dưỡng và tương tác thuốc.
- Khuyến cáo thời điểm lấy máu để xét nghiệm INR. - Các biện pháp xử trí khi kết quả INR cao ở người bệnh đang dùng thuốc chống đông kháng vitamin K không phụ thuộc vào tình trạng xuất huyết và hướng dẫn dẫn xử trí cấp cứu đảo ngược tác dụng của thuốc chống đông kháng vitamin K trong trường hợp quá liều. c) Kê đơn
- Bác sĩ kê đơn cần xác định xem người bệnh nữ trong độ tuổi sinh sản có đang mang thai hoặc đang cho con bú hay không. Nếu có đang nghi ngờ, nên chỉ định xét nghiệm thử thai trước khi kê đơn thuốc. - Chỉ định dùng chống đông và mục tiêu điều trị nên được ghi vào hồ sơ bệnh án/sổ khám bệnh. Thông tin bao gồm tên thuốc chống đông, liều lượng, thời gian điều trị dự kiến, dự kiến khung thời gian xem xét và đánh giá để quyết định điều chỉnh phác đồ chống đông nếu cần thiết. - Khi đánh giá nguy cơ thuyên tắc huyết khối tĩnh mạch, nên xác định người bệnh có đang dùng bất kỳ loại thuốc chống đông nào khác hay không. - Với bệnh nhân người lớn, độ thanh thải creatinin nên được ước tính theo công thức Cockcroft & Gault trước khi bắt đầu dùng thuốc chống đông thải trừ chính qua thận. d) Bảo quản và cấp phát
- Nên sử dụng heparin không phân đoạn dạng dung dịch pha sẵn nếu điều kiện cung ứng thuốc cho phép. - Các ống tiêm chứa heparin không phân đoạn đậm đặc dự trữ tạm thời, nên chuẩn bị ở dạng đơn liều. e) Sử dụng thuốc
- Nên có kiểm tra chéo việc sử dụng thuốc chống kháng vitamin K và các thuốc chống đông đường tiêm. f) Giám sát người bệnh
- Hướng dẫn theo dõi xuất huyết trong thời gian sử dụng thuốc như các xét nghiệm, theo dõi lâm sàng nên được ghi trong bệnh án hoặc sổ theo dõi sức khỏe người bệnh. - Người bệnh đang dùng thuốc chống đông nếu bị té ngã có thể làm tăng nguy cơ xuất huyết và chấn thương nghiêm trọng (bao gồm cả chấn thương sọ não). Do đó, cần theo dõi và giám sát chặt chẽ các người bệnh này. g) Phân tích sử dụng thuốc
Các người bệnh đang dùng thuốc chống đông nên được phân tích sử dụng thuốc để tối ưu hiệu quả điều trị và đảm bảo an toàn. h) Tư vấn/giáo dục cho người bệnh.
- Người bệnh hoặc người chăm sóc nên được cung cấp thông tin thuốc qua trao đổi trực tiếp và bằng văn bản. - Thông tin tư vấn và hướng dẫn nên bao gồm: - Tên và liều dùng của thuốc chống đông.
- Khoảng thời gian điều trị dự kiến và thời gian để bác sĩ chuyên khoa đánh giá lại.
- Hướng dẫn phát hiện biến cố xuất huyết và cách xử trí.
- Hướng dẫn trong trường hợp quên liều thuốc.
- Hướng dẫn các xét nghiệm và đánh giá lâm sàng cần thực hiện.
- Cảnh báo tương tác thuốc, tương tác thuốc-thức ăn và chế độ sinh hoạt ảnh hưởng đến phác đồ điều trị.
- Hướng dẫn bảo quản và sử dụng cụ thể với thuốc.
- Người bệnh và/hoặc người chăm sóc cần có cơ hội để trao đổi về liệu pháp chống đông với nhân viên y tế. - Người bệnh đang sử dụng thuốc chống đông kháng vitamin K nên được cung cấp sổ theo dõi kết quả xét nghiệm INR và kết quả điều trị. 3.2. Kali (đường tĩnh mạch)
Muối kali được sử dụng đường tĩnh mạch để xử trí hạ kali máu ở người bệnh không thể bổ sung điện giải đường uống hoặc khi cần bù kali nhanh chóng. Kali clorid là muối được sử dụng phổ biến nhất, bên cạnh đó còn có dạng muối phosphat và acetat của kali. Biến cố liên quan đến sử dụng kali đường tĩnh mạch có thể dẫn đến tử vong trên người bệnh. Các biến cố bất lợi liên quan đến sử dụng kali đường tĩnh mạch thường gặp bao gồm: - - Truyền tĩnh mạch kali clorid quá nhanh do dụng cụ giới hạn tốc độ truyền như bơm truyền bị hỏng hoặc do thiết lập sai tốc độ truyền.
- - Tiêm liều kali clorid đậm đặc (ví dụ: kali clorid 10%) do lấy nhầm thuốc, chẳng hạn như lấy nhầm ống kali clorid thay vì ống natri clorid 0,9% khi tiến hành đuổi khí trong đường truyền.
- - Không trộn đều khi thêm kali clorid đậm đặc vào dịch truyền trước khi tiến hành truyền, khiến cho kali clorid nồng độ vẫn còn cao được truyền vào cơ thể người bệnh.
Hướng dẫn dưới đây gợi ý những thao tác tối thiểu cần thực hiện để giảm thiểu nguy cơ khi sử dụng kali đường tĩnh mạch. Hướng dẫn này không đề cập đến các hướng dẫn lâm sàng về sử dụng kali đường tĩnh mạch trong điều trị. a) Chiến lược quản lý nguy cơ
Hội đồng Thuốc và điều trị của bệnh viện nên phê duyệt hướng dẫn sử dụng kali đậm đặc truyển tĩnh mạch, trong đó chứa các thông tin sau: - - Nhân viên y tế cần được đào tạo chuyên môn để kê đơn hoặc tiến hành thao tác truyền muối kali đường tĩnh mạch.
- - Hướng dẫn thao tác chuẩn bị và tiến hành truyền tĩnh mạch kali clorid và các muối kali đậm đặc khác.
- - Tốc độ truyền khuyến cáo, bơm truyền đạt tiêu chuẩn và theo dõi lâm sàng. Khuyến cáo tốc độ truyền kali clorid tối đa ở người trưởng thành là 10 mmol/giờ.
- - Khuyến cáo về nồng độ sử dụng ở trẻ em (nếu cần).
- - Quy trình cấp phát thuốc tiêm muối kali đậm đặc, bao gồm danh sách những khu vực được phép tồn trữ ống kali clorid.
- - Luôn có sẵn dung dịch kali clorid được pha sẵn để truyền tĩnh mạch, bao gồm danh sách những khu vực được phép tồn trữ kali clorid 40 mmol trong túi 100 mL.
- - Truyền kali đường tĩnh mạch với tốc độ lớn hơn 10 mmol/giờ cần thực hiện ở các khu vực có đủ điều kiện chăm sóc và theo dõi người bệnh (bao gồm theo dõi điện tâm đồ).
b) Kê đơn
- Ưu tiên sử dụng kali clorid đường uống để điều trị hạ kali máu, nếu điều kiện lâm sàng cho phép. - Cân nhắc các nguồn đầu vào kali của mỗi người bệnh, như nuôi ăn qua ống thông dạ dày, nuôi ăn qua tĩnh mạch, ăn uống thông thường và dịch bổ sung. - Đơn thuốc nên thể hiện hàm lượng dưới dạng milimol (mmol), không nên thể hiện dưới dạng miligram trên lít (mg/L) hoặc phần trăm (%). - Đơn thuốc nên viết đầy đủ tên loại muối được sử dụng (ví dụ: kali clorid). - Đơn thuốc không được viết tên thuốc dưới dạng kí hiệu hóa học. - Đơn thuốc cần ghi đầy đủ tốc độ truyền, đường dùng, nồng độ, hướng dẫn sử dụng. Đơn thuốc không có hướng dẫn về nồng độ hoặc tốc độ truyền cần được rà soát lại để bổ sung đầy đủ thông tin trước khi cấp phát hoặc sử dụng thuốc. - Không kê đơn kali truyền tĩnh mạch liều bolus hoặc liều truyền nhanh khẩn cấp.
c) Bảo quản và cấp phát
❖Dung dịch pha sẵn - Dịch truyền kali clorid pha sẵn nên được phân biệt rõ ràng so với các dịch truyền tĩnh mạch khác bằng nhãn hoặc bằng dải màu trên túi hay bất cứ dấu hiệu nào để dễ dàng nhận biết. - Nồng độ dịch truyền pha sẵn cần được mô tả dưới dạng milimol (mmol) trên tổng thể tích cuối cùng.
- Túi dịch truyền pha sẵn thể tích nhỏ không nên có đầu thêm thuốc hoặc nếu dịch truyền tự pha thì đầu thêm thuốc phải được khóa kín. - Khi cần sử dụng thuốc ở nồng độ không có sẵn trên thị trường, nên sử dụng thuốc được pha chế tập trung tại khoa Dược. - Trong trường hợp không sử dụng được dung dịch kali clorid pha sẵn và khoa Dược không triển khai tự pha chế, nhân viên y tế cần chuẩn bị dung dịch kali đường tĩnh mạch ngay tại nơi sử dụng và phải đảm bảo vô khuẩn. Nếu biện pháp này được áp dụng thường xuyên ở cơ sở, quy trình cần nêu rõ rủi ro và các biện pháp dự phòng trong việc cấp phát muối kali đậm đặc. - Dịch truyền tĩnh mạch pha sẵn chứa kali cần ghi nhãn rõ ràng và được xếp tách biệt với các dịch truyền có kích thước tương tự (ví dụ: natri clorid 0,9%). - Nơi bảo quản dịch truyền pha sẵn cần có dấu hiệu nhận viết rõ ràng. ❖Ống thuốc tiêm - Ống tiêm kali clorid và muối kali đậm đặc khác không nên lưu trữ trong buồng bệnh, mà chỉ được lưu trữ ở khoa Dược (trừ trường hợp đặc biệt tại các chuyên khoa có kinh nghiệm và được đào tạo về sử dụng kali dạng đậm đặc). - Ống tiêm kali clorid không được để sẵn trên xe tiêm vì có nguy cơ tiêm nhầm. - Nếu cần thiết, ống tiêm kali nồng độ trên 1 mmol/mL chỉ được tồn trữ ở khoa Dược, tách biệt khỏi các chế phẩm thuốc tiêm khác. ❖Khoa/phòng hồi sức tích cực, cấp cứu hoặc phòng mổ Tại các chuyên khoa hồi sức tích cực, cấp cứu hoặc phòng mổ, khi sử dụng kali liều cao và nồng độ cao cần lưu ý: - - Đánh giá rủi ro để xác định có nên tồn trữ ống thuốc ngay trong phòng hay không, và nếu có, nên tuân thủ quy trình an toàn trong chuẩn bị và sử dụng thuốc.
- - Nên giới hạn số loại nồng độ thuốc tiêm/truyền kali đậm đặc và không nên có nồng độ lớn hơn 1 mmol/mL.
- - Ống thuốc tiêm muối kali cần được xếp tách biệt khỏi các ống thuốc tiêm khác có hình dạng và bao bì tương tự (ví dụ: xếp trong hộp tách biệt có đánh dấu bằng màu và không được mở sẵn bao bì thuốc).
- - Nên có sẵn chế phẩm dung dịch đậm đặc thể tích nhỏ pha sẵn (ví dụ: 40 mmol/túi 100 mL).
d) Sử dụng thuốc - Khi có chỉ định dịch truyền kali đường tĩnh mạch, nên sử dụng dịch truyền kali clorid đường tĩnh mạch pha sẵn trên thị trường nếu điều kiện cho phép. - Nếu pha thêm muối kali vào dịch truyền tĩnh mạch, phải hòa trộn kĩ dung dịch bằng cách lắc ngược và lắc mạnh dung dịch ngay trước khi sử dụng. Không bao giờ được pha thêm dung dịch kali đậm đặc vào bịch dung dịch đang treo, do rất khó hòa trộn kĩ lượng kali đậm đặc và người bệnh có thể bị truyền kali nồng độ cao. - Cần dùng dụng cụ giới hạn tốc độ truyền như bơm truyền khi truyền tất cả các loại dung dịch chứa kali. Nên sử dụng bơm tự động có thể thiết lập sẵn chương trình truyền. - Nồng độ kali truyền qua đường truyền ngoại vi được khuyến cáo tối đa là 40 mmol/L đối với người lớn, trừ khi sử dụng dịch truyền pha sẵn trên thị trường (ví dụ: kali clorid 10 mmol/100 mL đẳng trương). Dung dịch nồng độ cao hơn cần được truyền qua thiết bị nối tĩnh mạch trung tâm. - Cần có người thứ hai kiểm tra, giám sát trong quá trình sử dụng các loại dịch truyền kali đường tĩnh mạch. 3.3. Methotrexat (dạng uống)
Methotrexat dạng uống được sử dụng trong điều trị các bệnh tự miễn hoặc tình trạng viêm như viêm khớp dạng thấp và bệnh vẩy nến nặng. Methotrexat cũng được sử dụng trong điều trị một số bệnh lý ung thư trong các phác đồ chuyên biệt. Methotrexat dạng uống thường được dùng một liều duy nhất 1 tuần/lần (tuy nhiên, đôi khi, nhằm cải thiện khả năng dung nạp trên một số người bệnh, tổng liều hàng tuần được chia thành 12 giờ/liều cho đến tối đa 3 liều/tuần). Chế độ liều 1 lần/tuần khác biệt so với các thuốc khác, đã dẫn đến sai sót khi sử dụng methotrexat dạng uống do bác sĩ và người bệnh thường quen thuộc với việc dùng thuốc hàng ngày. Các tác dụng không mong muốn đặc biệt nghiêm trọng liên quan đến độc tính của methotrexat có thể xảy ra sau khi sử dụng thuốc dạng uống hàng ngày thay vì dùng hàng tuần. Hướng dẫn dưới đây đưa ra các gợi ý với việc kê đơn, bảo quản, cấp phát và sử dụng methotrexat dạng uống một cách an toàn. Hướng dẫn này không bao gồm hướng dẫn lâm sàng về điều trị sử dụng methotrexat (dạng uống). a) Chiến lược quản lý nguy cơ
Hội đồng Thuốc và điều trị của bệnh viện nên phê duyệt hướng dẫn sử dụng thuốc bao gồm các thông tin sau: - Tiêu chuẩn theo dõi người bệnh đã được khuyến cáo.
- Truyền thông cho nhân viên y tế về nguy cơ liên quan đến việc sử dụng methotrexat dạng uống.
- Vai trò của người bệnh trong rà soát quy trình sử dụng thuốc.
b) Kê đơn
- Tiền sử dùng thuốc cần có thông tin về thời điểm dùng liều methotrexat cuối cùng. Bác sĩ nên tham khảo tiền sử dùng thuốc khi kê đơn methotrexat. - Tên thuốc methotrexat cần được viết đầy đủ. Không sử dụng các từ viết tắt như MTX. - Khi kê đơn liều hàng tuần, bác sĩ nên ghi rõ trên bảng kê thuốc hoặc đơn thuốc thông tin về: - Sử dụng methotrexat 1 tuần/lần (viết tên thuốc đầy đủ và không viết tắt).
- Có thông tin ngày dùng thuốc (ví dụ: Methotrexat 5 mg uống 1 tuần/lần vào THỨ BA).
- Người bệnh đang sử dụng methotrexat dạng uống nên tiếp tục được kê đơn methotrexat vào ngày người bệnh thường uống thuốc trong tuần trừ khi có lý do cần thiết phải thay đổi. Khi xuất viện, người bệnh và/hoặc người chăm sóc cần được thông báo thời điểm sử dụng liều methotrexat tiếp theo. - Bác sĩ nên gạch bỏ những ngày trên bảng theo dõi sử dụng thuốc khi không sử dụng methotrexat. - Khi sử dụng hệ thống quản lý thuốc tự động, nên xây dựng các cách thức cảnh báo để ngăn ngừa việc sử dụng methotrexat hàng ngày mà không theo mục tiêu cụ thể. - Trong một số chỉ định liên quan đến huyết học và ung thư, có thể kê đơn methotrexat với liều thường xuyên hơn. Vì vậy, bác sĩ nên bổ sung chỉ định điều trị trong các đơn thuốc có methotrexat đường uống. Điều này sẽ cảnh báo cho dược sĩ và điều dưỡng về các sai sót kê đơn có thể xảy ra khi dự định dùng thuốc 1 lần/tuần. c) Bảo quản và cấp phát
- Methotrexat dạng bào chế viên nén có sẵn 2 hàm lượng (2,5 mg và 10 mg), khoa Dược nên thực hiện các biện pháp giảm thiểu sai sót khi cấp phát. Các biện pháp phòng tránh có thể bao gồm sử dụng các biển cảnh báo trên kệ và tách riêng từng loại thuốc. - Viên methotrexat không nên lưu trữ tại các khoa ở dạng tủ trực hoặc trong danh mục thuốc cấp phát “ngoài giờ hành chính”. - Tất cả các đơn thuốc có methotrexat nên được rà soát bởi dược sĩ để xác nhận thời gian, liều dùng phù hợp và được ghi rõ ràng trước khi cấp phát thuốc. Với người bệnh nhập viện vào những thời điểm ngoài giờ hành chính, cần có biện pháp để đảm bảo dược sĩ trực rà soát được các đơn thuốc có methotrexat. Có thể tạm dừng việc sử dụng methotrexat cho đến khi dược sĩ rà soát đơn thuốc. - Methotrexat nên được cấp phát cho từng người bệnh theo đơn thuốc. Bao bì cần ghi rõ liều dùng, ngày dùng trong tuần và kèm theo cảnh báo thuốc gây độc tế bào. - Khoa Dược chỉ nên cấp phát số lượng thuốc cần thiết cho liều hàng tuần, ưu tiên cấp phát vào ngày sử dụng thuốc nếu điều kiện cho phép. d) Sử dụng thuốc
- Điều dưỡng cần có kiến thức về cách sử dụng methotrexat, thời gian dùng thuốc và các tác dụng không mong muốn để sử dụng methotrexat an toàn cho người bệnh nội trú. - Điều dưỡng nên xác nhận với người bệnh hoặc người chăm sóc về ngày dùng thuốc trong tuần, liều dùng và thời điểm lần cuối sử dụng thuốc trước khi dùng liều methotrexat tiếp theo. - Trường hợp đơn thuốc không rõ ràng hoặc điều dưỡng có trao đổi thêm về liều dùng, nên kiểm tra lại thông tin với bác sĩ hoặc dược sĩ trước khi cho người bệnh sử dụng. e) Rà soát đơn thuốc
Rà soát đơn thuốc bởi dược sĩ nên được thực hiện với người bệnh được kê đơn methotrexat. f) Giám sát người bệnh Nhân viên y tế cần có đủ kiến thực và kỹ năng để phát hiện các triệu chứng gợi ý dấu hiệu của ngộ độc hoặc không dung nạp methotrexat trên người bệnh. g) Tư vấn/giáo dục cho người bệnh
- Bác sĩ kê đơn và dược sĩ nên cung cấp thông tin và tư vấn cho người bệnh hoặc người chăm sóc, tốt nhất chuyển cho người bệnh một bản sao của tờ Hướng dẫn sử dụng methotrexat. - Thông tin tư vấn cho người bệnh có thể bao gồm: - Nhấn mạnh liều dùng 1 lần/tuần bằng cách xác định rõ ràng ngày nào trong tuần sử dụng thuốc (khi kê đơn liều hàng tuần). Cần nhấn mạnh không dùng liều bổ sung “khi cần thiết” để kiểm soát triệu chứng.
- Các lưu ý xử trí nếu quên liều.
- Thông tin về tầm quan trọng của xét nghiệm cần theo dõi thường xuyên, các triệu chứng ngộ độc và sự cần thiết can thiệp sớm nếu xuất hiện các triệu chứng.
- Nhấn mạnh việc người bệnh cần xác nhận với điều dưỡng giám sát ngày cần dùng thuốc trong tuần, liều dùng và thời điểm thuốc được dùng lần cuối trước khi dùng một liều methotrexat.
- Điều dưỡng cũng cần được trang bị kiến thức để cung cấp thông tin và tư vấn về methotrexat cho người bệnh. - Người bệnh hoặc người chăm sóc cần được cung cấp thông tin cụ thể về chế độ liều cho từng chỉ định và ngày trong tuần cần dùng thuốc. Ngoài các lưu ý cụ thể ở trên đối với việc sử dụng methotrexat dạng uống, khi cấp phát loại thuốc này, nhân viên y tế cần lưu ý các thông tin liên quan đến thuốc gây độc tế bào. 3.4. Vincristin
Vincristin là một thuốc chống ung thư nhóm alkaloid Dừa cạn có độc tính trên thần kinh. Việc tiêm nhầm vincristin đường tủy sống dẫn tới rối loạn thần kinh trung ương nghiêm trọng và thậm chí có thể gây tử vong. Hướng dẫn dưới đây gợi ý những yêu cầu tối thiểu cần thực hiện để dự phòng biến cố xảy ra khi sử dụng vincristin. Hướng dẫn này không bao gồm hướng dẫn lâm sàng về việc sử dụng vincristin trong điều trị. a) Chiến lược quản lý nguy cơ
Hội đồng Thuốc và điều trị của bệnh viện nên phê duyệt hướng dẫn sử dụng thuốc bao gồm các thông tin sau: - Nhấn mạnh chỉ những nhân viên y tế có kinh nghiệm và được đào tạo chuyên môn về điều trị ung thư có thể kê đơn, chuẩn bị, cấp phát hoặc sử dụng vincristin cho người bệnh. - Tách riêng quá trình hóa trị dùng đường tiêm tủy sống với các đường khác. Ví dụ: Dược sĩ yêu cầu bác sĩ xác nhận hoàn thành toàn bộ các phác đồ hóa trị dùng đường tiêm tủy sống trước khi tiêm tĩnh mạch vincristin cho người bệnh trong cùng ngày đó. Hoặc nếu có thể, chọn quy trình tách thuốc hóa trị dùng đường tiêm tủy sống và tiêm tĩnh mạch sử dụng trong các ngày khác nhau. b) Bảo quản và cấp phát
- Chuẩn bị và sử dụng liều vincristin trong một túi truyền. Không chuẩn bị trong bơm tiêm. - Tất cả chế phẩm vincristin, bao gồm cả bao bì bên ngoài nên được dán nhãn cảnh báo. Ví dụ: “CHỈ DÙNG TIÊM TĨNH MẠCH – CÓ THỂ GÂY TỬ VONG NẾU DÙNG ĐƯỜNG KHÁC”. Bao bì bên ngoài cũng nên ghi “Không tháo bỏ cho tới khi truyền”. c) Cấp phát, vận chuyển và sử dụng riêng biệt thuốc d&ugr
 HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)[/caption]
HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)[/caption] 
 VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH[/caption]
VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH[/caption] 
 b Khuyến cáo sử dụng thuốc cập nhật nhất, có thể tiếp cận được tính đến ngày cuối cùng kê đơn hay dùng thuốc của người bệnh. Nguồn khuyến cáo gồm có ít nhất 01 trong số các tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc được phê duyệt tại Việt Nam hoặc một số nước tham chiếu khác, hoặc Hướng dẫn chẩn đoán và điều trị được Bộ Y tế ban hành.a ADR được ghi nhận ở ít nhất 01 tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc (Anh/Hoa Kỳ/Pháp), Micromedex hoặc Hướng dẫn điều trị. c 1- Phòng tránh được (-13 đến -8 hoặc phát hiện được ít nhất 1 sai sót trong quy trình sử dụng thuốc); 2 – Có khả năng phòng tránh được (-7 đến -3) ; 3- Không đánh giá được (-2 đến 2) ; 4 – Không phòng tránh được (+3 đến +8).
b Khuyến cáo sử dụng thuốc cập nhật nhất, có thể tiếp cận được tính đến ngày cuối cùng kê đơn hay dùng thuốc của người bệnh. Nguồn khuyến cáo gồm có ít nhất 01 trong số các tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc được phê duyệt tại Việt Nam hoặc một số nước tham chiếu khác, hoặc Hướng dẫn chẩn đoán và điều trị được Bộ Y tế ban hành.a ADR được ghi nhận ở ít nhất 01 tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc (Anh/Hoa Kỳ/Pháp), Micromedex hoặc Hướng dẫn điều trị. c 1- Phòng tránh được (-13 đến -8 hoặc phát hiện được ít nhất 1 sai sót trong quy trình sử dụng thuốc); 2 – Có khả năng phòng tránh được (-7 đến -3) ; 3- Không đánh giá được (-2 đến 2) ; 4 – Không phòng tránh được (+3 đến +8). 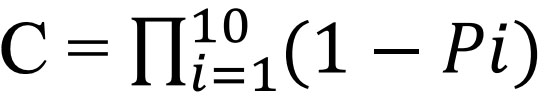 Trong đó: C là điểm hoàn thành của một cặp thuốc – ADR Pi là điểm phạt của mỗi trường thông tin bị thiếu (xem Bảng 9.1) + Các báo cáo không có thông tin về thuốc nghi ngờ và/hoặc không mô tả biểu hiện ADR được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). + Điểm hoàn thành của một báo cáo thấp nhất là 0 và cao nhất là 1. Báo cáo có điểm hoàn thành < 0,8 là báo cáo kém chất lượng và báo cáo có điểm hoàn thành từ 0,8 đến 1 điểm là báo cáo chất lượng tốt. Bảng 9.1. Điểm phạt các trường thông tin trong báo cáo ADR theo thang điểm VigiGrade 2
Trong đó: C là điểm hoàn thành của một cặp thuốc – ADR Pi là điểm phạt của mỗi trường thông tin bị thiếu (xem Bảng 9.1) + Các báo cáo không có thông tin về thuốc nghi ngờ và/hoặc không mô tả biểu hiện ADR được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). + Điểm hoàn thành của một báo cáo thấp nhất là 0 và cao nhất là 1. Báo cáo có điểm hoàn thành < 0,8 là báo cáo kém chất lượng và báo cáo có điểm hoàn thành từ 0,8 đến 1 điểm là báo cáo chất lượng tốt. Bảng 9.1. Điểm phạt các trường thông tin trong báo cáo ADR theo thang điểm VigiGrade 2  HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)[/caption]
HƯỚNG DẪN GIÁM SÁT PHẢN ỨNG CÓ HẠI CỦA THUỐC (ADR) TẠI CÁC CƠ SỞ KHÁM BỆNH, CHỮA BỆNH (Ban hành kèm theo Quyết định số 29/QĐ-BYT ngày 05 tháng 01 năm 2022)[/caption] 
 VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH[/caption]
VÍ DỤ MẪU BÁO CÁO ADR CÓ CHỦ ĐÍCH[/caption] 
 b Khuyến cáo sử dụng thuốc cập nhật nhất, có thể tiếp cận được tính đến ngày cuối cùng kê đơn hay dùng thuốc của người bệnh. Nguồn khuyến cáo gồm có ít nhất 01 trong số các tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc được phê duyệt tại Việt Nam hoặc một số nước tham chiếu khác, hoặc Hướng dẫn chẩn đoán và điều trị được Bộ Y tế ban hành.a ADR được ghi nhận ở ít nhất 01 tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc (Anh/Hoa Kỳ/Pháp), Micromedex hoặc Hướng dẫn điều trị. c 1- Phòng tránh được (-13 đến -8 hoặc phát hiện được ít nhất 1 sai sót trong quy trình sử dụng thuốc); 2 – Có khả năng phòng tránh được (-7 đến -3) ; 3- Không đánh giá được (-2 đến 2) ; 4 – Không phòng tránh được (+3 đến +8).
b Khuyến cáo sử dụng thuốc cập nhật nhất, có thể tiếp cận được tính đến ngày cuối cùng kê đơn hay dùng thuốc của người bệnh. Nguồn khuyến cáo gồm có ít nhất 01 trong số các tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc được phê duyệt tại Việt Nam hoặc một số nước tham chiếu khác, hoặc Hướng dẫn chẩn đoán và điều trị được Bộ Y tế ban hành.a ADR được ghi nhận ở ít nhất 01 tài liệu tham khảo theo thứ tự: Dược thư Quốc gia Việt Nam, Tờ hướng dẫn sử dụng thuốc (Anh/Hoa Kỳ/Pháp), Micromedex hoặc Hướng dẫn điều trị. c 1- Phòng tránh được (-13 đến -8 hoặc phát hiện được ít nhất 1 sai sót trong quy trình sử dụng thuốc); 2 – Có khả năng phòng tránh được (-7 đến -3) ; 3- Không đánh giá được (-2 đến 2) ; 4 – Không phòng tránh được (+3 đến +8). 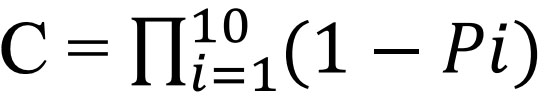 Trong đó: C là điểm hoàn thành của một cặp thuốc – ADR Pi là điểm phạt của mỗi trường thông tin bị thiếu (xem Bảng 9.1) + Các báo cáo không có thông tin về thuốc nghi ngờ và/hoặc không mô tả biểu hiện ADR được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). + Điểm hoàn thành của một báo cáo thấp nhất là 0 và cao nhất là 1. Báo cáo có điểm hoàn thành < 0,8 là báo cáo kém chất lượng và báo cáo có điểm hoàn thành từ 0,8 đến 1 điểm là báo cáo chất lượng tốt. Bảng 9.1. Điểm phạt các trường thông tin trong báo cáo ADR theo thang điểm VigiGrade 2
Trong đó: C là điểm hoàn thành của một cặp thuốc – ADR Pi là điểm phạt của mỗi trường thông tin bị thiếu (xem Bảng 9.1) + Các báo cáo không có thông tin về thuốc nghi ngờ và/hoặc không mô tả biểu hiện ADR được xếp vào nhóm không đủ điều kiện đánh giá (0 điểm). + Điểm hoàn thành của một báo cáo thấp nhất là 0 và cao nhất là 1. Báo cáo có điểm hoàn thành < 0,8 là báo cáo kém chất lượng và báo cáo có điểm hoàn thành từ 0,8 đến 1 điểm là báo cáo chất lượng tốt. Bảng 9.1. Điểm phạt các trường thông tin trong báo cáo ADR theo thang điểm VigiGrade 2